温馨提示: 药品图片来自网络,仅供参考;如遇新包装上市可能存在上新滞后,请以实物为准,如有侵权,请联系删除
本品主要有效成分为索托拉西布
其化学结构如下:
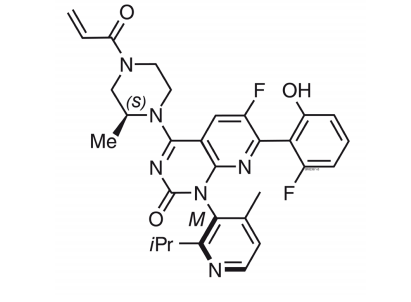
1.推荐剂量
(1)推荐剂量为960mg(8片),每天一次,直至疾病进展或出现不可接受的毒性
(2)如果漏服超过当日服药时间6小时以上,请跳过该剂量,第二天服药仍按照原剂量服用,不要同时服用2剂来弥补错过的剂量
(3)吞下整粒药片,不要咀嚼、压碎或分裂药片
2.建议的剂量减少

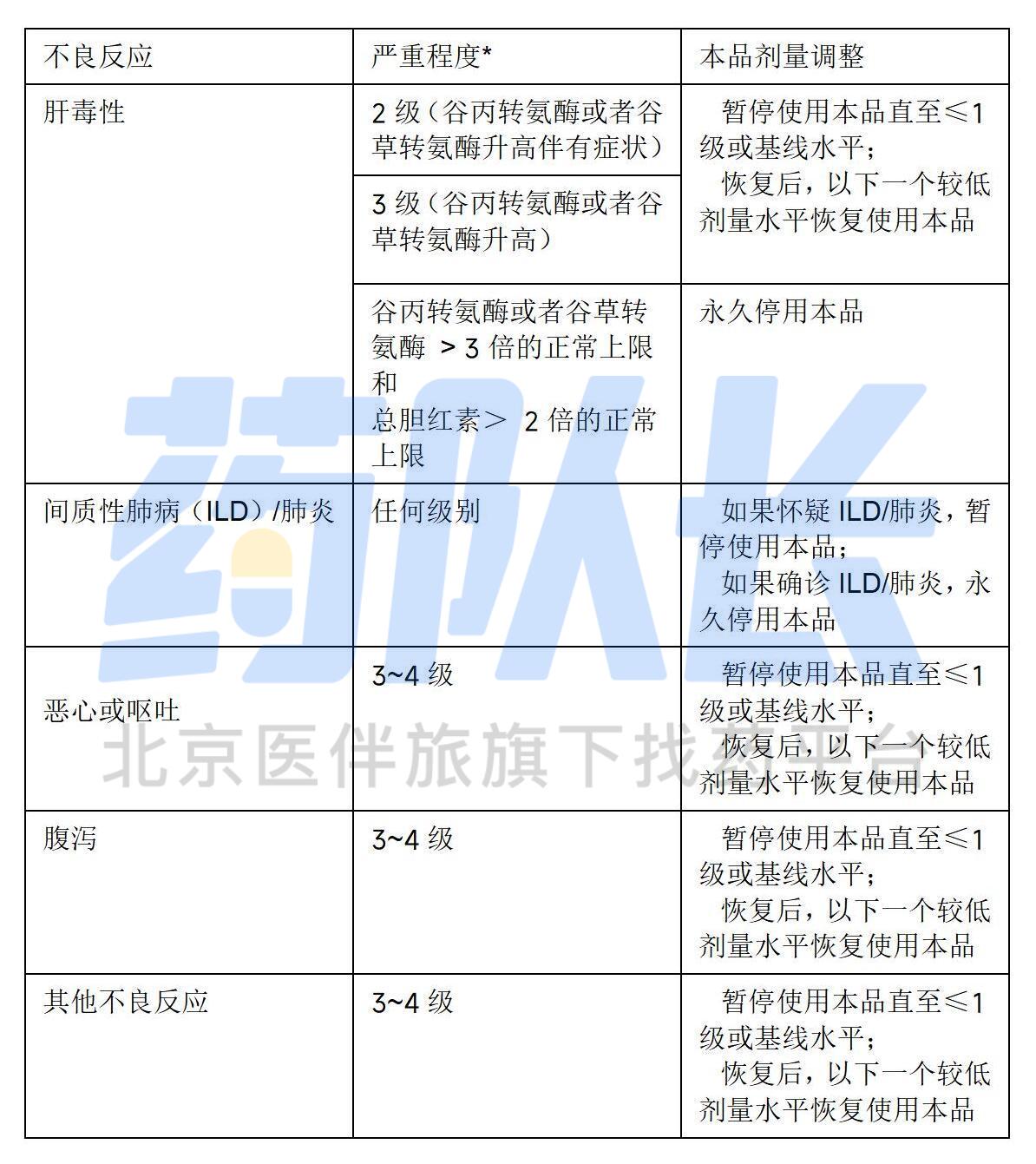
3.不良反应的推荐剂量调整
最常见的不良反应(≥20%)是腹泻、肌肉骨骼疼痛、恶心、疲劳、肝毒性和咳嗽
最常见的实验室异常(≥25%)为淋巴细胞减少、血红蛋白降低、天冬氨酸转氨酶升高、丙氨酸转氨酶升高、钙降低、碱性磷酸酶升高、尿蛋白升高和钠降低
1.肝毒性
使用本品治疗可能会引起肝损伤,开始用药后的前三个月,每3周监测一次肝功能;然后每月监测一次或根据临床指征,对出现转氨酶或胆红素升高的患者进行更频繁的监测;根据不良反应的严重程度,暂停、减少剂量或永久停用此药
2.间质性肺病(ILD)/肺炎
使用本品治疗可能会引起致命的间质性肺病,应监测新的或恶化的肺部症状,对于疑似ILD/肺炎,立即停用索托拉西布,如果未发现ILD/肺炎的其他潜在原因,则永久停用
(以上参考自FDA美国药监局英文说明书2023.04版)
免责声明: 以上内容整理于FDA、DRUGS、网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: FDA说明书,FDA更新于2025年1月的说明书https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=214665
- 药品知识
- 药品信息
- 聚焦索托拉西布靶向治疗KRAS G12C阳性非小细胞肺癌 新型KRAS G12C抑制剂索托拉西布(AMG 510)于2021年5...[ 详情 ]推荐指数:802 2022-05-07
- 索托拉西布(AMG510)用法用量 本文主要介绍了索托拉西布的推荐剂量、给药方法、吞咽固体有困难的病人给药...[ 详情 ]推荐指数:1000 2022-05-18
- 索托拉西布的副作用及不良反应 索托拉西布具有肝毒性,且可引起间质性肺病(ILD)/非感染性肺炎。...[ 详情 ]推荐指数:988 2022-06-01
- 2022WCLC|AMG 510联合疗法疾病控制率达100% 2022年世界肺癌大会于近日顺利召开,发布的研究中,AMG 510联合...[ 详情 ]推荐指数:1200 2022-08-12
-
【青光眼或高眼压症】DE-117B滴眼液
[适应症]原发性开角型青光眼或高眼压症[试验分期]Ⅲ期
-
【肝功能不全】LH-1801片
[适应症]肝功能不全[试验分期]Ⅰ期
-
【系统性红斑狼疮】C-CAR168细胞回输注射液
[适应症]系统性红斑狼疮[试验分期]Ⅱ期
-
【复发脑胶质瘤】GNC-039四特异性抗体注射液
[适应症]复发脑胶质瘤(病理确诊为四级星型细胞瘤和四级胶质母细胞瘤)[试验分期]Ⅰ期