ADC药物-DS8201治疗非小细胞肺癌获美国药监局批准
8月11日,美国药监局(FDA)批准DS8201(德喜曲妥珠单抗、Enhertu)用于治疗HER2突变的转移性或不可切除性非小细胞肺癌(NSCLC),这是在HER2突变非小细胞肺癌中,获批的首款ADC药物(抗体药物偶联物),而在此前,DS8201已有多个适应症获得中美药监局突破性疗法认定。

美国药监局(FDA)标志性建筑物
什么是突破性疗法认定?
突破性疗法认定(BTD)早于2017年7月,由FDA首次提出,目前中国药监局(NMPA)在《药品管理法》也包含该程序。突破性疗法认定是加速罕见病或严重疾病,以及威胁生命的新药研发和审批的一种措施。
DS8201的突破性疗法认定
美国药监局
1.2017年8月29日—治疗既往接受过曲妥珠单抗和帕妥珠单抗及T-DM1治疗后疾病进展、HER2阳性局晚期或转移性乳腺癌;
2.2020年5月12日—治疗HER-2阳性、不可切除的或转移性胃癌或胃食管连接部腺癌;
3.2020年5月18日—治疗HER2突变的转移性或不可切除的非小细胞肺癌;
4.2021年10月4日—治疗既往接受过≥1种抗HER2治疗的不可切除的或转移性HER2阳性乳腺癌。
中国药监局
2022年4月1日,DS8201用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性乳腺癌成人患者,获中国药监局突破性疗法认定。
什么是HER2突变?
HER2突变,也可称为HER2阳性,多由生长因子受体2基因突变所致,肺癌、乳腺癌等多种癌症中,都有可能存在HER2基因异常突变,往往对酪氨酸激酶抑制剂(TKI),一种靶向抗癌药原发性耐药。原发性耐药是指对某个或某类药物治疗无反应,仅在六个月内就会出现耐药,通常需要寻找其他药物治疗。
目前,市面上绝大多数靶向药是TKI药物,如乐伐替尼、奥希替尼等,因此,HER2基因突变检测为阳性的患者,对绝大多数靶向治疗无效,亟需特效靶向药物。
ADC药物的作用原理和特点
ADC药物一般是由特异性单克隆抗体和高杀伤性细胞毒性药物,通过特定的连接头,从而将靶标偶联起来的靶向生物药剂,其目的是“瞄准”目标肿瘤细胞,更精准地把小分子细胞毒性药物运输到目标肿瘤细胞,再由小分子细胞毒性药物“毒死”肿瘤细胞。
ADC药物结合高抗肿瘤活性细胞毒性药物,以及靶向性、选择性强的抗体的优势,既具有小分子细胞毒性药物的肿瘤杀伤特性,又能够选择性降低该类药物脱靶的副作用,更高效地发挥药物的治疗作用。
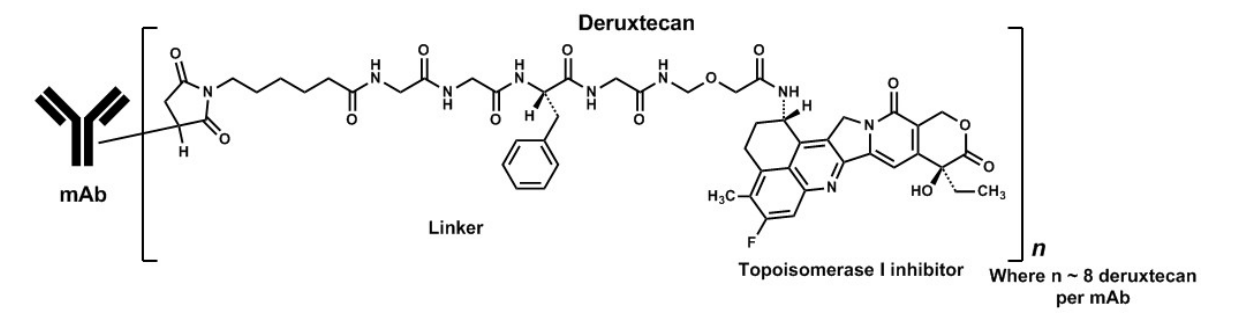
DS8201结构图
DS8201为何被称为“神药”?
DS8201是一款靶向HER2的ADC药物,由英国阿斯利康和日本第一三共联合研发,是曲妥珠单抗(赫赛汀、Trastuzumab)和依沙替康,通过肽链构成的复合药物,同时兼具靶向药和化疗药的优点,能够治疗对TKI原发性耐药的HER2突变转移性、复发性或不切除的肺癌、乳腺癌、胃癌以及结直肠癌,这类患者多处于晚期,DS8201因可作为多种晚期癌症的治疗选择,因此被称为“神药”。

DS8201 英国阿斯利康 100mg
DESTINY-Lung02—DS8201治疗HER2突变非小细胞肺癌客观缓解率近60%!
DESTINY-Lung02研究是一项多中心、随机的II期临床试验,Daiichi Sanky教授等人在此研究中,评估了DS8201治疗HER2突变的转移性或不可切除的非小细胞肺癌的疗效和安全性。
试验设计
研究共纳入了52例HER2阳性的转移性或不可切除的非鳞状非小细胞肺癌患者,每3周接受DS8201 5.4mg/kg静脉注射一次,直至出现不可接受的毒性或发生疾病进展。
疗效结果
客观缓解率(ORR):所有患者的ORR为57.7%,1.9%的患者(1例)达到完全缓解,55.8%的患者(29例)为部分缓解;
中位缓解持续时间(DOR):8.7个月。
安全性结果
最常见的实验室检查异常(≥20%):白细胞、中性粒细胞、血红蛋白、淋巴细胞、血小板和白蛋白减少,天冬氨酸氨基转移酶、丙氨酸氨基转移酶和碱性磷酸酶升高;
最常见的不良反应(≥20%)):恶心呕吐、食欲下降、疲劳、便秘和脱发。
研究证实,DS8201治疗HER2突变的非小细胞肺癌具有持久的抗癌活性,近六成患者出现缓解,且绝大多数不良反应可耐受,这一试验直接推动了DS8201在肺癌中的获批。
HER2突变癌症治疗,HER2检测是关键
癌症治疗逐渐向精准治疗发展,ADC药物也是该时代背景下的产物,精准医疗归根结底离不开临床诊断和临床检查。只有明确药物的适用患者人群,少走反复尝试的弯路,才能更早地控制患者病情的发展,发挥药物的最佳疗效。
多项研究证实,DS8201对HER2突变的患者更加有效。目前,临床上最常用的HER2检测方法是荧光原位杂交法(FISH)以及免疫组织化学法(IHC),想要接受DS8201治疗的患者,一定要去专业机构进行检测。
中国药监局已受理DS8201的上市申请
目前,DS8201还未在国内上市,2022年3月21日,我国药监局已受理DS-8201在中国的上市申请,目前仍在审批过程中。
不止在肺癌,DS8201作为一款“新星”药物,用于乳腺癌的治疗,出现缓解的患者超过60%,晚期胃癌中,有效率也超过50%,对结直肠癌的疾病控制率(DCR)甚至高达83%,DS8201作为一款高效且多面的ADC药物,在中国上市指日可待!
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm