温馨提示: 药品图片来自网络,仅供参考;如遇新包装上市可能存在上新滞后,请以实物为准,如有侵权,请联系删除。
普乐沙福
1、推荐剂量及给药方法
(1)在患者接受每日一次的G-CSF治疗4天后,开始使用普乐沙福治疗,在开始每次血液透析前约11小时使用普乐沙福,最多连续使用4天
(2)普乐沙福皮下注射的推荐剂量基于体重
①体重小于或等于83kg的患者:20mg固定剂量或0.24mg/kg
②体重大于83公斤的患者:0.24mg/kg
③使用患者的实际体重计算普乐沙福的给药量,每瓶可提供1.2毫升20毫克/毫升的溶液,患者的给药量应根据以下公式计算:
0.012 × 患者实际体重(kg) = 给药量(ml)
(3)在临床研究中,普乐沙福的剂量是根据患者的实际体重来计算的,体重不超过理想体重的175%,尚未对体重超过理想体重175%的患者的普乐沙福剂量和治疗进行研究
(4)根据随体重增加而增加的暴露量,普乐沙福剂量不应超过40mg/天
(5)在给药之前,应目视检查药瓶是否有颗粒物质和变色,如果有颗粒物质或溶液变色,则不应使用
(6)丢弃未使用的部分
2、推荐的伴随药物
在晚间首次使用普乐沙福之前的4天内,以及在进行血液透析之前的每一天,每天早上使用G-CSF 10ug/kg
3、肾损害的剂量调整
对于中度和重度肾功能损害患者(估计肌酐清除率(CLCR)小于或等于50 mL/min),应根据体重类别将普乐沙福的剂量减少三分之一,如表1所示,如果肌酐清除率小于或等于50 mL/min,剂量不应超过27 mg/天,因为以mg/kg为基础的剂量会导致普乐沙福暴露量随体重增加而增加,与肾功能正常的受试者相比,如果中度和重度肾功能损害患者的剂量减少1/3,预计会有类似的全身暴露量
表1:普乐沙福在肾损害患者中的推荐剂量
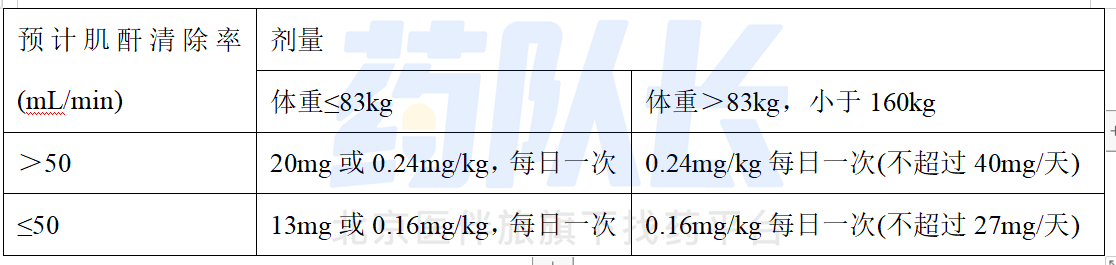
以下公式可用于估算肌酐清除率(CLCR):
①男性
肌酐清除率(mL/min) =体重(kg) ×(140 -年龄)÷(72 ×血清肌酐(mg/dL))
②女性
肌酐清除率(mL/min)=0.85×男性计算值
目前还没有足够的信息来推荐血液透析患者的剂量
最常见的不良反应(≥10%):腹泻、恶心、疲劳、注射部位反应、头痛、关节痛、头晕、呕吐
1、过敏性休克和超敏反应
在普乐沙福给药期间和给药后至少30分钟观察患者的过敏症状,直到每次给药结束后临床稳定,只有在人员和治疗方法可立即用于治疗过敏反应和其他超敏反应时,才可使用普乐沙福
2、白血病患者肿瘤细胞动员
对于造血干细胞的动员,普乐沙福可能会导致白血病细胞的动员,进而污染血液制品,因此,普乐沙福不适用于白血病患者的造血干细胞动员和采集
3、血液影响
(1)白细胞增多
普乐沙福与G-CSF联合使用可增加循环白细胞和HSC(肝星状细胞)数量,在使用普乐沙福期间监测白细胞计数
(2)血小板减少
在服用普乐沙福的患者中观察到血小板减少,监测所有接受普乐沙福后进行单采的患者血小板计数
4、肿瘤细胞移动的潜力
当普乐沙福与G-CSF联合用于造血干细胞动员时,肿瘤细胞可能会从骨髓中释放出来,随后被收集到白细胞生成物中,肿瘤细胞可能再灌注的影响尚未得到充分研究
5、脾肿大及破裂
如果接受普乐沙福与G-CSF联合治疗的患者报告左上腹痛和/或肩胛或肩部疼痛,则对其脾脏完整性进行评估
6、胚胎-胎儿毒性
妊娠女性使用本品时可能危害胎儿,建议育龄女性在本品给药期间有效避孕,如果妊娠期间使用该药物,或者患者在使用该药物期间发生妊娠,应告知患者对胎儿的潜在危害
7、对驾驶和操作机器能力的影响
本品可能影响驾驶和操作机器能力,部分患者出现眩晕,疲乏或血管迷走神经反应,因此,驾驶和操作机器时应谨慎
(以上内容均参考自美国FDA官网普乐沙福说明书英文版 2020.08)
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm。
- 药品知识
- 药品信息
- 普乐沙福适应症和用法用量 普乐沙福与粒细胞集落刺激因子(G-CSF)联合用于调动造血干细胞(HS...[ 详情 ]推荐指数:667 2022-05-27
- 普乐沙福的不良反应和注意事项 接受普乐沙福联合粒细胞集落刺激因子(G-CSF)的患者在调动造血干细胞...[ 详情 ]推荐指数:522 2022-05-27
-
【青光眼或高眼压症】DE-117B滴眼液
[适应症]原发性开角型青光眼或高眼压症[试验分期]Ⅲ期
-
【肝功能不全】LH-1801片
[适应症]肝功能不全[试验分期]Ⅰ期
-
【系统性红斑狼疮】C-CAR168细胞回输注射液
[适应症]系统性红斑狼疮[试验分期]Ⅱ期
-
【复发脑胶质瘤】GNC-039四特异性抗体注射液
[适应症]复发脑胶质瘤(病理确诊为四级星型细胞瘤和四级胶质母细胞瘤)[试验分期]Ⅰ期