试验概述
SOLAR-1(NCT02437318)是一项随机、双盲、安慰剂对照试验,对572名HR阳性、HER2阴性、晚期或转移性乳腺癌患者(其疾病在基于芳香化酶抑制剂的治疗(含或不含CDK4/6组合)或治疗后进展或复发)进行了实验组(阿培利司加氟维司群)与对照组(安慰剂加氟维司群)的对比研究。如果患者患有炎症性乳腺癌、1型糖尿病或未控制的2型糖尿病或肺炎,则被排除在外。根据是否存在肺转移和/或肝转移,以及之前是否使用CDK4/6抑制剂治疗,对随机分组进行分层。
试验内容
患者连续每天口服一次阿培利司(300 mg)或安慰剂,并在第1周期、第1天和第15天以及每28天周期的第1天肌注氟维司群(500 mg)。患者接受治疗,直到影像学疾病进展或出现不可接受的毒性为止。前18个月每8周进行一次肿瘤评估,之后每12周进行一次。
患者的中位年龄为63岁(范围为25至92岁)。大多数患者为女性(99.8%),大多数患者为白人(66%),其次是亚裔(22%)、其他未知人群(10%)、黑人或非裔美国人(1.4%)和美洲印第安人或阿拉斯加人(0.9%)。基线ECOG表现状态为0(68%)或1(32%)。
大多数患者(98%)接受过激素治疗作为最后一次治疗(48%转移治疗,52%辅助治疗)。13%的患者观察到原发性内分泌抵抗(定义为辅助内分泌治疗24个月内复发或晚期疾病内分泌治疗6个月内进展)和继发性内分泌抵抗(定义为辅助内分泌治疗24个月后复发,辅助内分泌治疗结束后12个月内复发),72%的患者在接受内分泌治疗6个月后出现进展。
试验指标
主要疗效结果是研究者评估的实体瘤(RECIST)v11.中PIK3CA突变符合反应评估标准的队列无进展生存率(PFS)。其他疗效结果指标是PIK3CA突变队列的总有效率(ORR)和总生存率(OS)。
试验结果
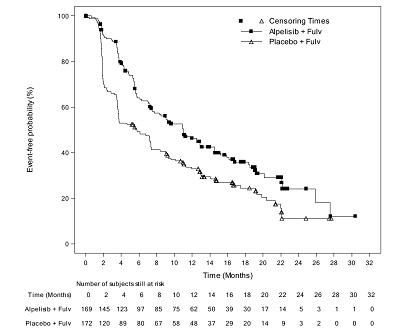
肿瘤组织中PIK3CA突变队列的疗效结果图1所示。研究者评估的PIK3CA突变队列的PFS结果得到了盲法独立审查委员会(BIRC)评估的一致结果的支持。在组织或血浆PIK3CA突变的患者中观察到一致的结果。在进行最终PFS分析时,27%(92/341)的患者已死亡,总体存活率随访尚不成熟。
试验结果显示,实验组的中位无进展生存期(PFS)(95% CI)为11.0月(范围7.5-14.5),比对照组的无进展生存期(5.7个月(范围3.7-7.4))高出5.3个月。二者的风险比(95% CI)为0.65(0.50,0.85)。实验组的客观缓解率ORR(95% CI)为35.7个月(范围27.4,-44.7) ,是对照组客观缓解率(16.2个月(范围10.4-23.5))的两倍有余。总的来说,阿培利司加氟维司群组的生存率较安慰剂加氟维司群组有显著的提高。
图1:SOLAR-1的无进展生存期(研究者评估PIK3CA肿瘤突变)分析图如下:
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: FDA说明书,FDA更新于2024年04月24日的说明书https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=218466