1 / 1
Rx
康奈非尼
别称:恩考芬尼、康奈芬尼、Encorafenib、Braftovi
温馨提示: 药品图片来自网络,仅供参考;如遇新包装上市可能存在上新滞后,请以实物为准,如有侵权,请联系删除
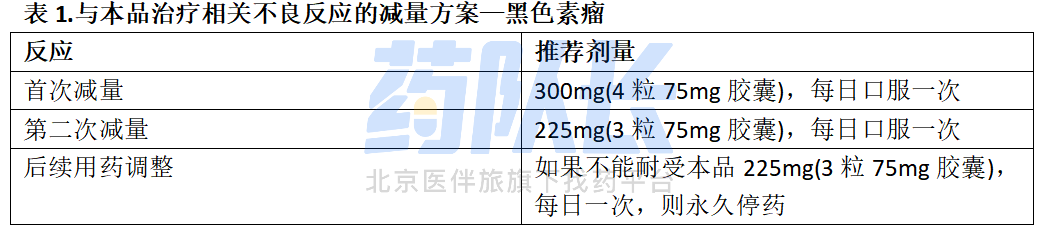
1.BRAF V600E或V600K突变阳性不可切除或转移性黑色素瘤
本品适用于与比美替尼联合治疗经FDA批准的检测,确认存在BRAF V600E或V600K突变的不可切除或转移性黑色素瘤患者。
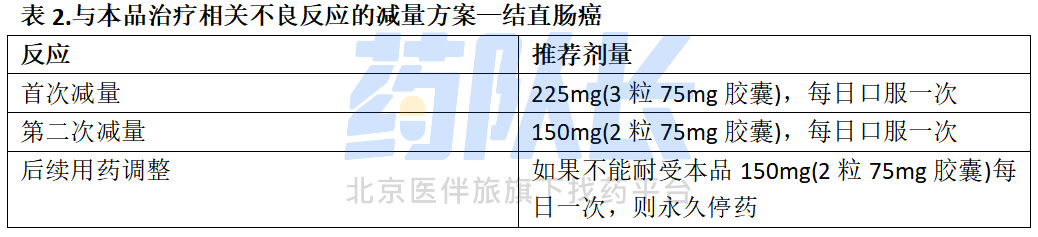
2.BRAF V600E突变阳性转移性结直肠癌(CRC)
本品适用于与西妥昔单抗联合治疗经FDA批准的检测,确认存在BRAF V600E突变、既往接受过治疗的转移性结直肠癌成人患者。
3.使用限制
本品不适用于野生型BRAF黑色素瘤或野生型BRAF结直肠癌患者的治疗。
免责声明: 以上内容整理于FDA、DRUGS、网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: FDA说明书,FDA更新于2024年12月的说明书https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=210496
- 药品知识
- 药品问答
- 康奈非尼的适应症是什么? 康奈非尼是一种用于治疗黑色素瘤和结直肠癌的药物,其适应症主要包括以下情...[ 详情 ]推荐指数:260 2023-09-19
- 康奈非尼的注意事项是什么? 康奈非尼是一种常用于治疗黑色素瘤和结直肠癌的靶向治疗药物。在使用康奈非...[ 详情 ]推荐指数:247 2023-09-19
- 治疗黑色素瘤和结直肠癌的有效药物-康奈非尼的副作用大吗? 最近很多病友咨询这个康奈非尼,很多病友很关心这个副作用方面的问题,俗话...[ 详情 ]推荐指数:269 2023-08-02
- 康奈非尼治疗黑色素瘤可延长患者生命近10个月!价格如何? 最近很多患者看到了康奈非尼在治疗黑色素瘤上的效果,想知道这个药物202...[ 详情 ]推荐指数:671 2023-08-03
临床招募 新药免费用
-
【青光眼或高眼压症】DE-117B滴眼液
[适应症]原发性开角型青光眼或高眼压症[试验分期]Ⅲ期
-
靶向新药!PI3Kα抑制剂 招募卵巢癌、输卵管癌、腹膜癌患者
[适应症]适用症复发/持续性卵巢、输卵管或原发性腹膜透明细胞癌[试验分期]Ⅱ期
-
免费治疗!CD20 CAR-T细胞疗法 招募阳性非霍奇金淋巴瘤患者
[适应症]复发/难治性CD20阳性B细胞非霍奇金淋巴瘤(B-NHL),包括:弥漫大B细胞淋巴瘤(DLBCL,包括组织学转化型)和转化型滤泡性淋巴瘤(TFL)[试验分期]Ⅰ期
-
免费新药!抗体偶联药物 招募CD20阳性B细胞非霍奇金淋巴瘤患者
[适应症]复发或难治的CD20阳性B细胞非霍奇金淋巴瘤[试验分期]Ⅰ期