艾拉司群(Orserdu)适应症是什么
艾拉司群(Orserdu)是一种新型雌激素受体拮抗剂,2023年获得美国FDA批准上市,为特定基因突变型晚期乳腺癌患者提供了精准治疗选择。该药物通过独特的分子机制作用于雌激素信号通路,在克服内分泌治疗耐药方面展现出显著临床优势。
艾拉司群(Orserdu)适应症是什么
主要适应症范围
(1)、艾拉司群适用于治疗经FDA批准检测方法确认存在ESR1突变的雌激素受体阳性、HER2阴性的晚期或转移性乳腺癌的绝经后女性或成年男性患者。
(2)、适用人群需满足在至少一线内分泌治疗后出现疾病进展的条件。
患者筛选标准
(1)、选择接受艾拉司群治疗的患者必须基于ESR1突变状态进行严格筛选。
(2)、突变检测应使用FDA批准的检测方法,通过血浆样本进行分析确定。
艾拉司群(Orserdu)药物规格特性
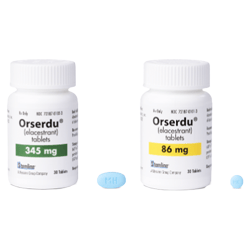
345毫克片剂
(1)、外观呈浅蓝色、椭圆形,双凸状,一面刻有“MH”字样,另一面为空白。
(2)、每片相当于400毫克艾拉司群盐酸盐(即约含345毫克艾拉司群游离碱)。
86毫克片剂
(1)、外观为浅蓝色、圆形,双凸状,一面刻有“ME”字样,另一面为空白。
(2)、每片相当于100毫克艾拉司群盐酸盐(即约含86毫克艾拉司群游离碱)。
成分
(1)、两种规格的片剂均含有以下非活性成分:二氧化硅胶体、交聚维酮、硬脂酸镁(非动物源)、微晶纤维素、硅化微晶纤维素等。
(2)、包衣成分包括聚乙烯醇、二氧化钛、聚乙二醇、FD&C蓝1号及滑石粉。
艾拉司群(Orserdu)储存条件
环境温度控制
(1)、艾拉司群应在20°C至25°C(68°F至77°F)的标准室温环境下储存。
(2)、允许在15°C至30°C(59°F至86°F)范围内进行短期存放。
包装规格说明
(1)、药物以供应的包装规格为每瓶30片,采用儿童安全盖密封。
(2)、345毫克片剂的国家药品编码为NDC72187-0102-3。
(3)、86毫克片剂的国家药品编码为NDC72187-0101-3。

艾拉司群是一种雌激素受体拮抗剂,适用于:
绝经后妇女或成年男性,ER阳性、HER2阴性、ESR1突变的晚期或在至少一种内分泌治疗后疾病进展的转移性乳腺癌。