来特莫韦(Prevymis)的说明书
来特莫韦于2017年在美国首次上市,目前已经在国内上市,并且顺利进入医保报销范畴,大大减轻了患者的经济负担及购买负担,本文就来特莫韦的适应症、用法用量、副作用、禁忌、临床疗效等进行了详细说明。
(一)适应症
1.预防造血干细胞移植(HSCT)患者巨细胞病毒感染
来特莫韦适用于预防巨细胞病毒(CMV)血清反应阳性的异基因造血干细胞移植(allo-HSCT)成人受者(R+)的巨细胞病毒感染以及相关疾病。
2.预防肾移植受者巨细胞病毒感染
来特莫韦适用于预防高危成人肾移植患者(患者CMV血清阳性/CMV血清阴性[D+/R-])的巨细胞病毒感染和相关疾病。
来特莫韦
(二)用法用量
1.推荐剂量
(1)来特莫韦的推荐剂量为480mg,每日口服或静脉注射一次,与环孢素合用时应调整用药剂量。
(2)在患者进行造血干细胞移植(HSCT)的第0天和第28天之间(移植前或移植后)开始用药治疗,持续用药到造血干细胞移植(HSCT)后的第100天。如果药物用于有晚期巨细胞病毒感染和疾病风险的患者,用药可持续到造血干细胞移植(HSCT)后200天。
(3)来特莫韦用于肾移植患者时,在移植后第0天和第7天之间开始用药,并持续用药到移植后第200天。
2.用药注意事项
(1)来特莫韦口服剂可以与或不与食物一起服用,但需要整片吞下,不可咀嚼或压碎。
(2)来特莫韦注射剂必须通过0.2μm或0.22μm的无菌聚醚砜(PES)在线过滤器进行注射,通过外周导管或中心静脉管线以恒定速率静脉输注给药超过1小时,且不能作为静脉推注给药。
(3)来特莫韦注射液应仅用于无法接受口服治疗的患者,一旦患者能够服用口服药物,就应该改用可以口服的来特莫韦片剂,来特莫韦片剂和注射剂可根据医生的判断互换使用,在转换剂型时无需调整剂量。
(4)在完成用药预防后,建议造血干细胞移植(HSCT)患者进行巨细胞病毒再激活监测。
3.漏服补充
如果患者漏服一剂药物,需要尽快补服,如果直到下次服药时才想起漏服,在下次计划的时间正常服药即可,不要连续服用两剂药物。
4.剂量调整
(1)如果来特莫韦口服剂或注射剂与环孢素同时给药,来特莫韦的剂量应减少至240mg,每天一次。
(2)如果环孢素是在预防用药后开始使用,来特莫韦的下一次剂量应减少到240mg,每天一次。
(3)如果在开始用药后停用环孢素,下一次来特莫韦的剂量应增加至480mg,每天一次。但如果是因为患者体内环孢素水平高而中断环孢素的用药,则无需调整来特莫韦的剂量。
5.来特莫韦注射剂的制备
来特莫韦注射液以30ml单剂量小瓶提供,每小瓶含240mg/12ml(20mg/ml)或480mg/24ml(20mg/ml),任一剂量的制备和给药说明都相同,制备要求如下:
(1)来特莫韦样品瓶仅供一次性使用,使用后要丢弃任何未使用的剩余部分,在静脉注射使用前必须稀释来特莫韦,日常不要摇晃药物试剂瓶。
(2)来特莫韦注射液是一种无色透明的溶液,可能含有一些与产品相关的半透明或白色小颗粒。稀释来特莫韦前检查小瓶内容物是否存在变色和颗粒物质,如果溶液混浊、变色或含有少量半透明或白色小颗粒以外的物质,请勿使用。
(3)不要将来特莫韦注射液与含有增塑剂邻苯二甲酸二乙基己酯(DEHP)的静脉注射袋和输液器材料一起使用,仅使用不含DEHP的静脉注射袋和输液器材料,不含邻苯二甲酸酯的材料通常也不含DEHP。
(4)制备药物时,需要将一瓶来特莫韦注射液加入一个250ml预装静脉注射袋中,袋中含有0.9%氯化钠注射液(美国药典)或5%葡萄糖注射液(美国药典),轻轻混合,不要摇晃。只有0.9%的氯化钠和5%的葡萄糖在化学和物理上与来特莫韦注射液相容。
(5)来特莫韦一旦稀释溶液透明,可能从无色到黄色,在此范围内的颜色变化不会影响产品质量。给药前应目视检查药物是否有颗粒物质和变色,如果稀释溶液混浊、变色或含有除少数半透明或白色小颗粒以外的物质,需要丢弃。稀释溶液在室温下可保存24小时,在2°C至8°C的冷藏条件下可保存48小时(该时间包括输注期间稀释溶液在静脉注射袋中的储存时间)。
(6)稀释的溶液必须通过0.2μm或0.22μm的无菌聚醚砜(PES)在线过滤器给药,不要通过除0.2μm或0.22μm无菌PES在线过滤器之外的过滤器给药。在1小时内,通过外周导管或中心静脉导管以恒定速率静脉输注静脉注射袋中的全部内容物。
(7)来特莫韦注射液与盐酸胺碘酮、两性霉素B(脂质体)、氨曲南、盐酸头孢吡肟、环丙沙星、环孢素、盐酸地尔硫䓬、非格司亭、硫酸庆大霉素、左氧氟沙星、利奈唑胺、劳拉西泮、盐酸咪达唑仑、盐酸霉酚酸酯、昂丹司琼、帕洛诺司琼在物理上不相容。
(三)适用人群
成人,儿童、孕妇、哺乳期女性及老年人请在医生指导下使用。
(四)禁忌
1.服用匹莫齐特或麦角生物碱的患者禁用来特莫韦
(1)匹莫齐特
接受匹莫齐特治疗的患者同时使用来特莫韦,可能会导致匹莫齐特的浓度增加,因为来替莫韦抑制细胞色素P4503A(CYP3A),可能导致QT间期延长和尖端扭转型室性心动过速。
(2)麦角生物碱
服用麦角生物碱的患者同时服用来特莫韦可能导致麦角生物碱(麦角胺和二氢麦角胺)浓度增加,因为来特莫韦会抑制细胞色素P4503A(CYP3A),这可能导致患者出现麦角中毒。
2.与环孢素合用时禁用匹伐他汀和辛伐他汀
来特莫韦与环孢素合用可能导致匹伐他汀或辛伐他汀浓度显著升高,可能引起肌病或横纹肌溶解。
(五)副作用
1.造血干细胞移植(HSCT)患者
最常见的不良反应是恶心、腹泻、呕吐、外周水肿、咳嗽、头痛、疲劳和腹痛。
2.肾移植患者
最常见的不良反应是腹泻。
(六)注意事项
1.药物相互作用导致不良反应或疗效降低的风险
来特莫韦与某些药物合用可能会导致潜在的重大药物相互作用,其中一些可能会导致不良反应或药物的治疗效果降低,具体可以参考禁忌以及药物相互作用一栏。
(七)治疗效果
1.试验设计
本试验是一项单中心、回顾性的试验研究,研究对象为接受护理的537名连续巨细胞病毒感染(CMV)血清阳性的同种异体造血干细胞移植(HSCT)患者。
2.试验结果的设定
主要研究结果是探讨来特莫韦一级预防对试验人群难治性或耐药性巨细胞病毒感染的发生率和结果的影响。
3.试验结果
莱特莫韦一级预防可有效预防难治性或耐药性巨细胞病毒感染,并降低造血干细胞移植(HSCT)48周时患者的非复发死亡率以及巨细胞病毒相关疾病。
(八)药物相互作用
1.其他药物对来特莫韦的影响
(1)OATP1B1/3转运蛋白抑制剂
来特莫韦是OATP1B1/3和P-gp转运蛋白和UGT1A1/3酶的底物,与OATP1B1/3转运蛋白抑制剂药物合用可能导致来特莫韦血浆浓度升高,也可能导致OATP1B1/3转运蛋白抑制剂的血浆浓度升高。
OATP1B1/3转运蛋白抑制剂包括血管紧张素Ⅱ受体拮抗剂(沙坦类)、血管紧张肽转换酶抑制剂和抗糖尿病类药物(列奈类)。
(2)P-gp诱导剂
不建议将来特莫韦与P-gp诱导剂和或UGT诱导剂同时给药,因为有可能降低来替莫韦的血浆浓度。
P-gp诱导剂包括苯巴比妥(镇静催眠药、抗惊厥)、贯叶连翘(燥湿止带、消肿排脓、止血),UGT诱导剂包括利福平(抗结核)、苯妥英(抗癫痫、抗心律失常、三叉神经痛{精神类})等。
2.来特莫韦对其他药物的影响
(1)咪达唑仑
由于来特莫韦是CYP3A的中度抑制剂,来特莫韦与咪达唑仑合用可增加咪达唑仑的血浆浓度。
(2)CYP3A底物
来特莫韦与CYP3A底物药物合用,可能会导致合用的CYP3A底物的血浆浓度出现升高现象,CYP3A底物包括地西泮、劳拉西泮(镇静催眠、抗焦虑)等。
(3)环孢素
当来特莫韦与环孢素同时给药时,CYP3A和OATP1B1/3介导的药物相互作用的程度可能不同。有关来特莫韦与环孢素相互作用的信息,请参见环孢素的药物说明书。
3.已确定的来特莫韦和其他潜在重大药物的相互作用
具体请参考禁忌一栏以及表1,如果合并用药的剂量调整是由于使用来特莫韦治疗所致,则应在使用来特莫韦治疗完成后重新调整剂量。
表1-1.潜在的重大药物相互作用
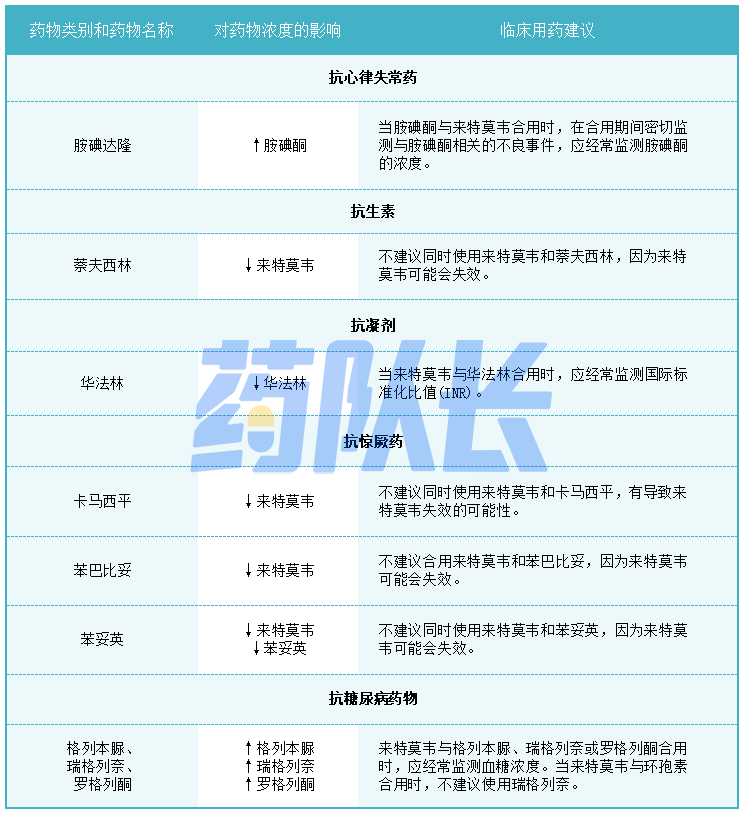
表1-2.潜在的重大药物相互作用
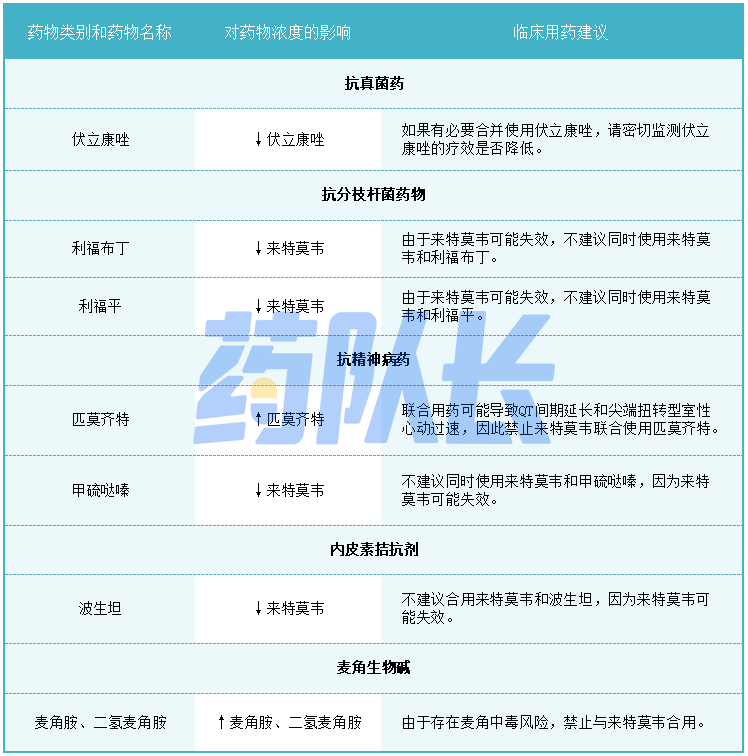
表1-3.潜在的重大药物相互作用
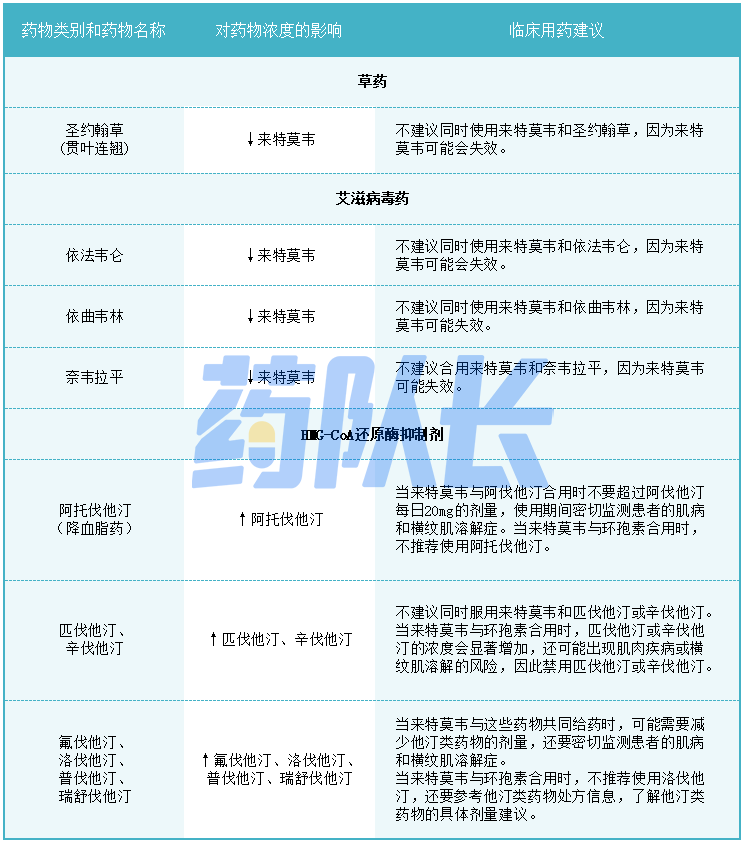
表1-4.潜在的重大药物相互作用
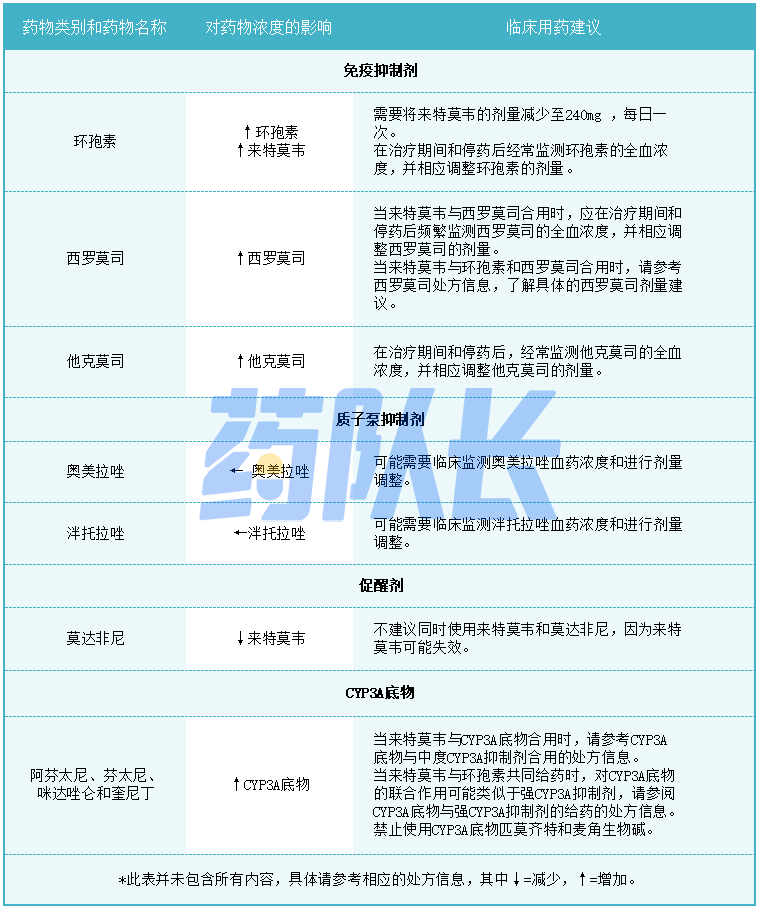
4.与来特莫韦物无临床显著相互作用的药物
在来特莫韦与阿昔洛韦、地高辛、霉酚酸酯、氟康唑、伊曲康唑、泊沙康唑、乙炔雌二醇和左炔诺孕酮的临床药物相互作用研究中,未观察到具有临床意义的相互作用。
(九)储存条件
将来特莫韦片剂和注射剂储存在20℃至25℃下,允许偏差为15℃-30℃,储存在原纸箱及原包装中,避免暴露在光线下。
【温馨提示】:部分商品说明书更换频繁,请以商品实物为准。


1.预防造血干细胞移植(HSCT)患者巨细胞病毒感染
来特莫韦适用于预防巨细胞病毒(CMV)血清反应阳性的异基因造血干细胞移植(allo-HSCT)成人受者(R+)的巨细胞病毒感染以及相关疾病。
2.预防肾移植受者巨细胞病毒感染
来特莫韦适用于预防高危成人肾移植患者(患者CMV血清阳性/CMV血清阴性[D+/R-])的巨细胞病毒感染和相关疾病。