阿达格拉西布简介
阿达格拉西布又名adagrasib、Krazati 、MRTX-849,2022年12月经美国药监局批准上市。
阿达格拉西布是第二款用于治疗KRAS G12C突变的局部晚期或转移性非小细胞肺癌的口服抑制剂,获得了优先审查权和孤儿药身份(1)。
此外,中国观察阿达格拉西部单药治疗和联合用药的治疗非小细胞肺癌的试验(CTR20221225)正在进行中,期待后续的结果以及药物在中国的上市。

药队长阿达格拉西布正面实拍图
阿达格拉西布治疗非小细胞肺癌的试验
阿达格拉西布的获批时基于一项多中心、单臂、开放标签的扩展队列研究(NCT03785249),研究对象是局部晚期或转移性KRAS G12C突变的非小细胞肺癌,之前接受过基于铂的治疗和免疫检查点抑制剂的治疗。
试验结果
客观缓解率43%,这意味着服用药物的患者有4成多肿瘤缩小了30%以上或完全消失且维持了一段时间。
疾病控制率79.5%,这说明了服用本药的患者有近8成肿瘤不变或出现了缩小。
中位无进展生存期6.5个月,这代表着半数患者服用本药后,疾病没有出现恶化或复发时间达到6.5个月。
中位总生存期12.6个月,这证明了半数患者服用本药后,生存时间延长了一年多。
试验数据表明患者服用阿达格拉西布治疗非小细胞肺癌疗效优越。
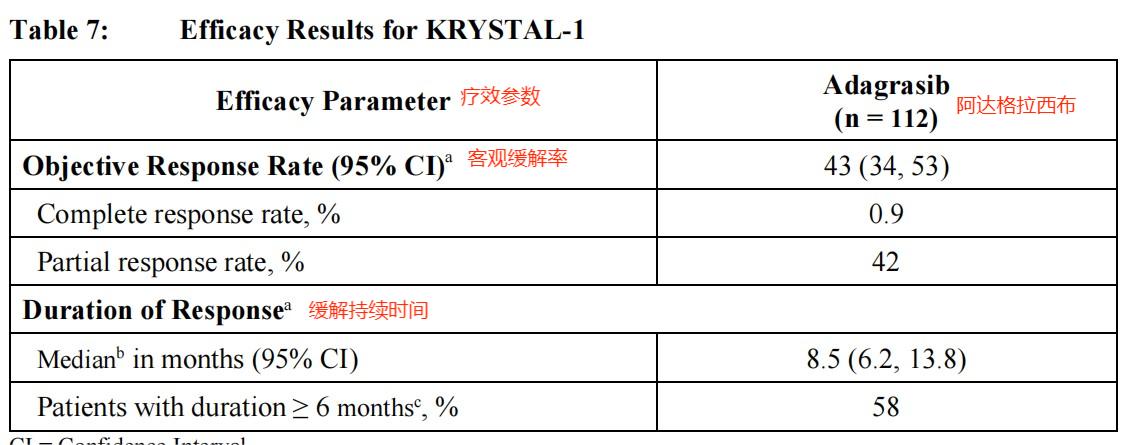
美国药监局官网阿达格拉西布说明书临床试验疗效截图
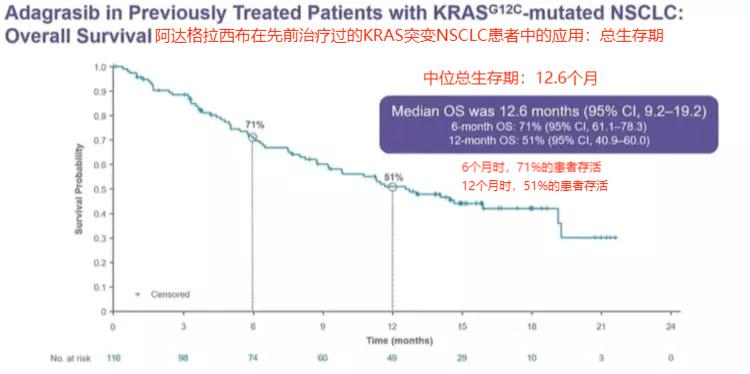
2022 ASCA年会发布的数据
安全性
在本试验中,最常见的不良反应(≥20%)为腹泻、恶心、疲劳、呕吐、肌肉骨骼疼痛、肝毒性、肾功能损害、呼吸困难、水肿、食欲下降、咳嗽、肺炎、头晕、便秘、腹痛和QTc间期延长。
严重不良反应(≥2%)为肺炎(17%)、呼吸困难(9%)、肾损害(8%)、败血症(5%)、缺氧(4.3%)、胸腔积液(4.3%)、呼吸衰竭(4.3%)、贫血(3.4%)、心力衰竭(3.4%)、低钠血症(3.4%)、低血压(3.4%)、肌无力(3.4%)、热射病(3.4%)、脱水(2.6%)、腹泻(2.6%)、精神状态改变(2.6%)、肺栓塞(2.6%)和肺出血(2.6%)。
因为试验患者中位年龄为64岁,年龄偏大,且疾病为经过一次治疗的非小细胞肺癌患者,自身情况和症状都比较特殊;出现的不良反应虽然多,但大部分都在可接受的范围内;因此阿达格拉西布的不良反应被认为是可耐受的。
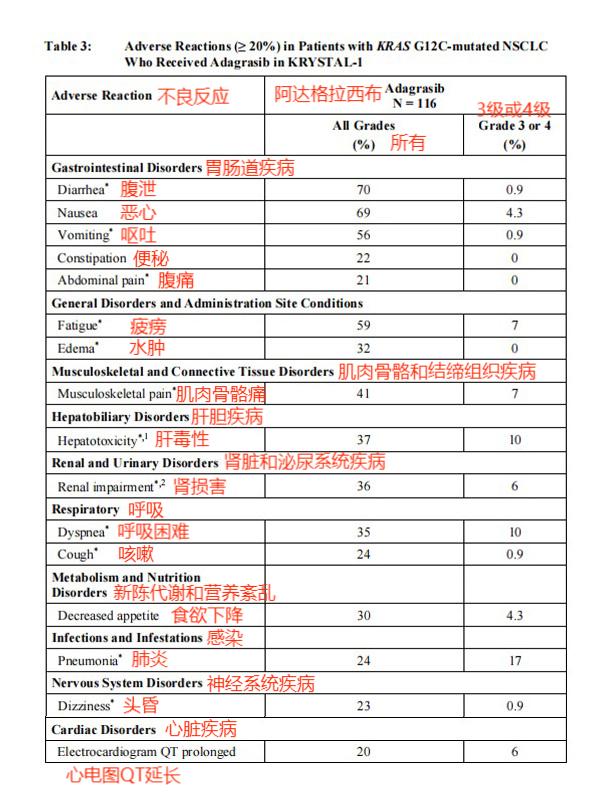
美国药监局官网阿达格拉西布不良反应数据截图
试验结论
KRAS G12C突变的局部晚期或转移性非小细胞肺癌的成年患者服用阿达格拉西布疗效优越,且安全性可耐受。

Pasi A.Jänne 丹娜法伯癌症研究所Lowe胸腔肿瘤学中心主任
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: FDA说明书,FDA更新于2024年6月21日的说明书https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=BasicSearch.process&ApplNo=216340