胰腺癌是恶性程度最高的癌症,五年存活率仅为5%,十分难治。2015年10月,法国servier公司研发的伊立替康脂质体注射液(liposome、安能得)获美国药监局(FDA)批准,为胰腺癌患者带来了新的曙光,该药可联合5-氟尿嘧啶(5-FU)和亚叶酸(LV),用于吉西他滨(泽菲、Gemzar)治疗后进展的转移性胰腺癌(mPC)患者,今年4月,中国药监局(NMPA)传来好消息,伊立替康脂质体获批在中国上市。
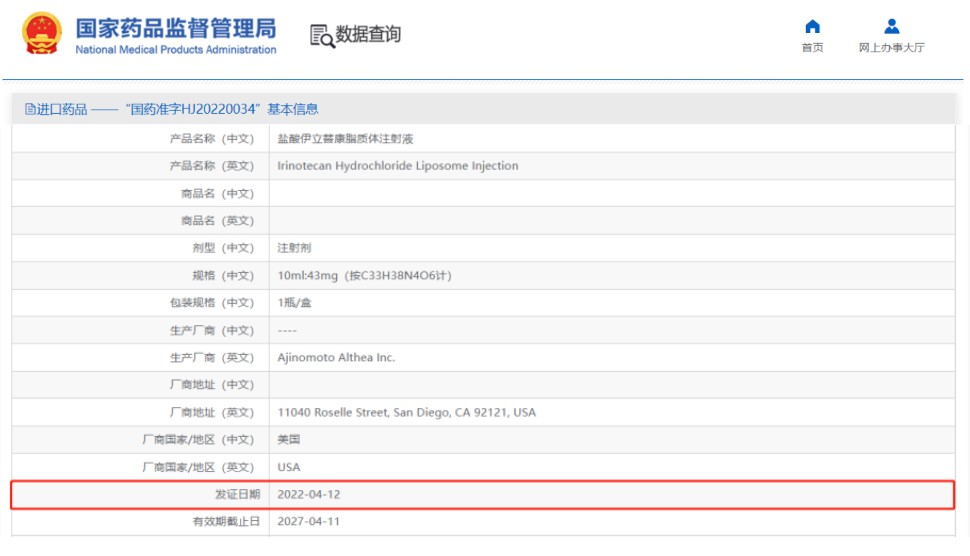
国家药监局伊立替康脂质体上市信息
9月,在第47届欧洲肿瘤内科学会(ESMO)上,公布了伊立替康脂质体在中国人群中开展的III期临床试验的最终数据,进一步证实中国胰腺癌患者接受伊立替康脂质体治疗,临床疗效十分可观。

欧洲肿瘤内科学会图片
伊立替康脂质体有哪些优势?
目前,伊立替康脂质体联合5-FU/LV是吉西他滨治疗后,发生进展的转移性胰腺癌的标准治疗之一,脂质体是药物的一种剂型,是将药物成分包裹在类脂质双分子层中,并形成微型泡囊,相较于伊立替康注射液(开普拓、艾力),该剂型:
1.具有淋巴导向性和靶向性,可精准打击肿瘤细胞;
2.包裹在泡囊中,可降低药物的毒性;
3.显著提高药物稳定性,从而提升疗效。
伊立替康 美国辉瑞 5ml和伊立替康脂质体 法国servier 43mg/10ml
欧洲肿瘤内科学会:伊立替康脂质体治疗局晚期胰腺癌,患者寿命延长2.4个月
今年欧洲肿瘤内科学会上,仁济医院的王理伟教授公布了伊立替康脂质体联合5-FU/LV(治疗组)对比安慰剂联合5-FU/LV,治疗局晚期胰腺癌(LAPC)患者疗效和安全性的III期临床试验的最终结果。

仁济医院的王理伟教授
该试验共纳入了298例吉西他滨治疗失败的患者,主要终点为总生存期(OS),中位随访12.81个月后,达到了主要终点,治疗组的中位总生存期为7.39个月,对照组仅为4.99个月,治疗组和对照组的中位无进展生存期(mPFS)分别为4.21个月和1.48个月。
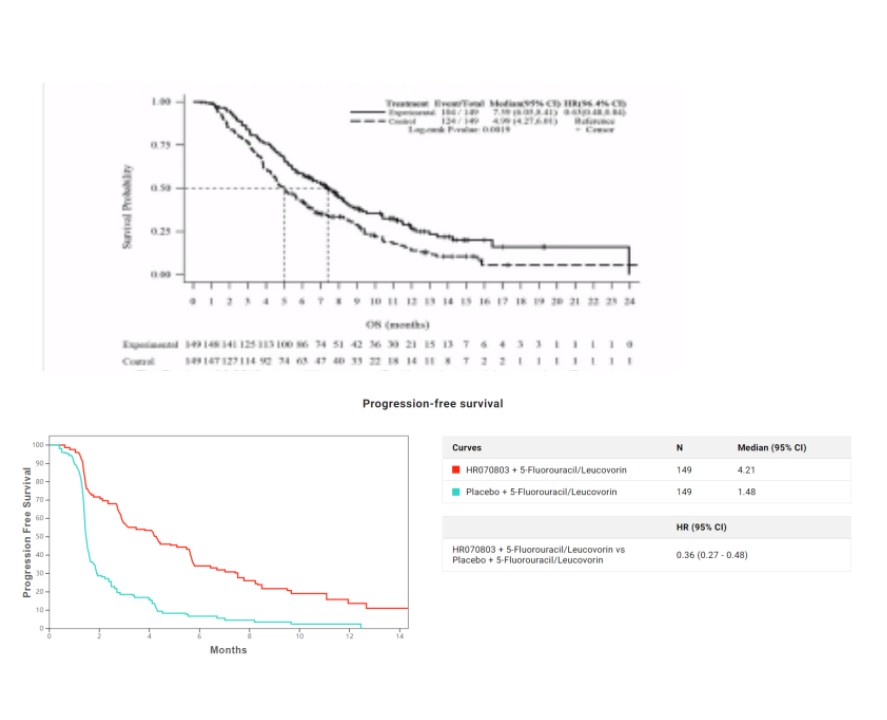
患者的总生存期(上)和无进展生存期(下)
在对安全性进行分析时,治疗组中最常见的≥3级不良事件中,19.05%的患者γ-谷氨酰转移酶(γ-GGT)升高,12.93%的患者发生中性粒细胞减少症,而对照组有33.33%的患者发生,远高于治疗组。此外,在对照组中还有1.36%的患者出现胆碱能综合征,而在治疗组中未观察到。
吉西他滨 美国礼来Lilly 200mg
研究发现,在吉西他滨治疗失败的局晚期或转移性胰腺癌患者中,使用伊立替康脂质体联合5-FU/LV治疗方案,能够改善患者生存,伊立替康脂质体使患者寿命延长了2.4个月,并且具有可控的安全性,这表明伊立替康脂质体联合5-FU/LV同样适用于中国人群,治疗局晚期胰腺癌可使患者具有明显的临床获益。
伊立替康脂质体的价格如何?进医保了吗?
目前,伊立替康脂质体注射液尚未进入我国医保目录,患者虽然可以在医院和药店购买,但无法享受医保价格。
市面上,法国servier公司研发的伊立替康脂质体注射液规格为43mg/10ml,售价在13200$左右,价格还是比较昂贵的,但未来或许能有医保相关的调整,以惠及广大胰腺癌患者。
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm