舒尼替尼(SUNITINIB)的说明书
目前舒尼替尼(SUNITINIB)已在国内上市。舒尼替尼是一种新型多靶向性的治疗肿瘤的口服药物,主要功效包括抑制肿瘤血管生成和抗肿瘤细胞生长,同时也可以作用于血管内皮生长因子受体、血小板源性生长因子受体、胃肠道间质瘤相关酪氨酸激酶、神经营养因子受体等多个靶点,被广泛用于治疗肾细胞癌、胃肠间质瘤以及胰腺神经内分泌肿瘤等实体瘤。本文就舒尼替尼的适应症、用法用量、副作用、禁忌、临床疗效等进行了详细说明。
(一)适应症
1.胃肠道间质瘤
舒尼替尼用于对甲磺酸伊马替尼治疗进展或不耐受的胃肠道间质瘤(GIST)成年患者。
2.晚期肾细胞癌
舒尼替尼用于成年晚期肾细胞癌(RCC)患者的治疗。
3.肾细胞癌的辅助治疗
舒尼替尼适用于肾切除术后肾细胞癌复发风险高的成年患者的辅助治疗。
4.晚期胰腺神经内分泌肿瘤
舒尼替尼适用于进行性、分化良好的胰腺神经内分泌肿瘤(pNET)的成人患者,伴有不可切除的局部晚期或转移性疾病。

舒尼替尼
(二)用法用量
1.胃肠道间质瘤和晚期肾细胞癌的推荐剂量
胃肠道间质瘤(GIST)和晚期肾细胞癌(RCC)的推荐剂量为50mg,每日口服一次,治疗4周,然后休息2周(即4/2给药方案),直到疾病进展或不可接受的毒性。舒尼替尼可与食物一起或不与食物一起服用。
2.肾细胞癌(RCC)辅助治疗的推荐剂量
舒尼替尼辅助治疗RCC的推荐剂量为50mg,每日口服一次,治疗4周,休息2周(即4/2给药方案),共9个6周的治疗周期。舒尼替尼可与食物一起或不与食物一起服用。
3.胰腺神经内分泌肿瘤(pNET)的推荐剂量
舒尼替尼治疗胰腺神经内分泌肿瘤(pNET)的推荐剂量为37.5mg,每日口服一次,直至疾病进展或不可接受的毒性。舒尼替尼可与食物一起或不与食物一起服用。
4.不良反应的剂量调整
为了控制不良反应,表1提供了推荐的剂量调整。表2提供了针对不良反应的舒尼替尼推荐减量。
表1:针对不良反应舒尼替尼的剂量调整
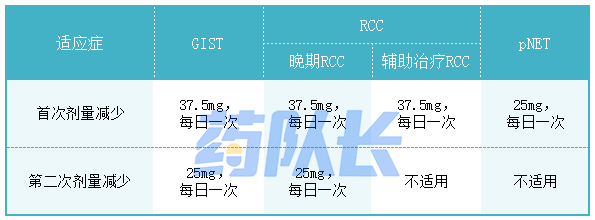
表2:针对不良反应舒尼替尼的推荐减量
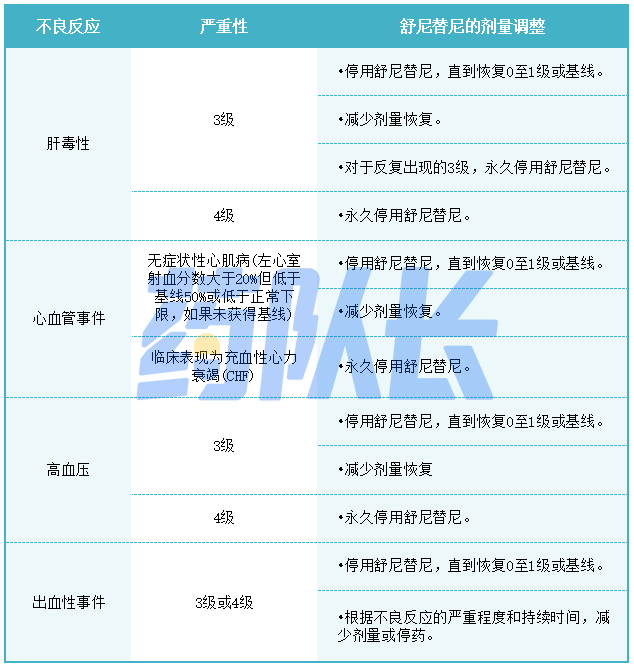
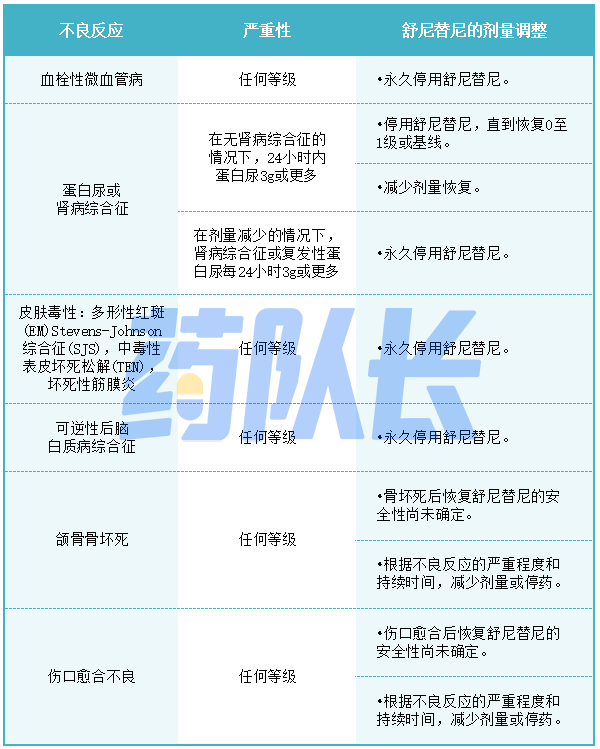
5.药物相互作用的剂量调整
⑴强CYP3A4抑制剂
选择一种没有或只有很小的酶抑制潜力的替代伴随药物。如果不能避免舒尼替尼与强CYP3A4抑制剂同时给药,可以考虑将舒尼替尼的剂量减少到最小剂量,如下所示:
①GIST和RCC:37.5mg口服,每日一次,治疗4周,休息2周(即4/2给药方案)。
②pNET:25mg口服,每日一次。
⑵强CYP3A4诱导剂
选择一种无酶诱导潜能或酶诱导潜能极小的替代伴随药物。如果不能避免舒尼替尼与强CYP3A4诱导剂同时给药,可以考虑将舒尼替尼的剂量增加到最大剂量,如下所示:
①GIST和RCC:87.5mg口服,每日一次,治疗4周,休息2周(即4/2给药方案)。
②pNET:62.5mg口服,每日一次。
③如果舒尼替尼剂量增加,应仔细监测患者的不良反应。
6.终末期肾病患者血液透析剂量的调整
终末期肾病(ESRD)血液透析患者不需要调整起始剂量。然而,考虑到与肾功能正常患者相比暴露量减少,基于安全性和耐受性,后续剂量可逐渐增加至2倍。
(三)适用人群
成人。妊娠期、哺乳期女性,儿童以及老年患者在医生指导下用药。
(四)禁忌症
尚不明确。
(五)副作用
最常见的不良反应(≥25%)是疲劳/乏力、腹泻、粘膜炎/口腔炎、恶心、食欲下降/厌食、呕吐、腹痛、手足综合征、高血压、出血事件、味觉障碍/味觉改变、消化不良和血小板减少。
(六)注意事项
1.肝毒性
⑴舒尼替尼可引起严重的肝毒性,导致肝功能衰竭或死亡。肝功能衰竭包括黄疸、转氨酶升高和/或高胆红素血症合并脑病、凝血功能障碍和/或肾功能衰竭。
⑵在每个治疗周期,监测肝功能测试(谷丙转氨酶[ALT],谷草转氨酶[AST],胆红素)在基线,并根据临床指示。中断3级肝毒性的舒尼替尼治疗,直到缓解到≤1级或基线,然后以减少剂量恢复舒尼替尼治疗。
⑶4级肝毒性患者、3级肝毒性未缓解的患者、随后肝功能检查发生严重变化的患者以及有其他肝衰竭体征和症状的患者停用舒尼替尼。ALT或AST>2.5倍正常值上限(ULN)或>5倍正常值上限并伴有肝转移的患者的安全性尚未确定。
2.心血管事件
⑴已有报道心血管事件的发生,包括心力衰竭、心肌病、心肌缺血和心肌梗死,其中一些是致命的。在使用舒尼替尼前12个月内出现心脏事件的患者,如心肌梗死(包括严重/不稳定型心绞痛)、冠状动脉/外周动脉旁路移植术、症状性CHF、脑血管意外或短暂性脑缺血发作或肺栓塞,均被排除在舒尼替尼临床研究之外。既往使用蒽环类药物或心脏放疗的患者也被排除在一些研究之外。目前尚不清楚合并这些疾病的患者发生左心室功能障碍的风险是否更高。
⑵考虑在基线监测LVEF,并根据临床指示定期监测。仔细监测患者的临床体征和充血性心力衰竭(CHF)的症状。有慢性心力衰竭临床表现的患者停用舒尼替尼。对于射血分数大于20%但低于基线值50%的无临床证据的CHF患者或未获得基线射血分数低于正常下限的患者,中断舒尼替尼和/或减少剂量。
3.QT间期延长和尖端扭转型室性心动过速
⑴舒尼替尼可导致QT间期以剂量依赖性方式延长,这可能导致室性心律失常(包括扭转角性心律失常)的风险增加。监测QT间期延长风险较高的患者,包括有QT间期延长病史的患者,正在服用抗心律失常药物的患者,或已有相关心脏病、心动过缓或电解质紊乱的患者。考虑在使用舒尼替尼治疗期间定期监测心电图和电解质(即镁、钾)。
⑵当舒尼替尼与强CYP3A4抑制剂或已知延长QT间期的药物同时使用时,更频繁地监测QT间期。考虑减少剂量。
4.高血压
根据临床指征监测基线血压。酌情启动和/或调整降压治疗。对于3级高血压患者,在缓解至≤1级或基线之前,暂停使用舒尼替尼,然后减少剂量恢复舒尼替尼。4级高血压患者停用舒尼替尼。
5.出血事件和内脏穿孔
⑴出血性事件包括胃肠道、呼吸道、肿瘤、泌尿道和大脑,其中一些是致命的。在接受舒尼替尼治疗的患者中观察到肿瘤相关出血。这些事件可能突然发生,在肺肿瘤的情况下,可能表现为严重和危及生命的咯血或肺出血。在接受舒尼替尼治疗的转移性RCC、GIST和转移性肺癌患者中观察到肺出血,其中一些有致命的结果。舒尼替尼未被批准用于肺癌患者。
⑵据报道,在接受舒尼替尼治疗的腹内恶性肿瘤患者中出现了严重、有时甚至致命的胃肠道并发症,包括胃肠道穿孔。进行连续全血细胞计数(CBCs)和身体检查以及出血事件的临床评估。对于3级或4级出血事件中断舒尼替尼治疗,直到缓解至≤1级或基线水平,然后以减少的剂量恢复舒尼替尼治疗。3级或4级出血事件未得到解决的患者应停用舒尼替尼。
6.肿瘤溶解综合征
肿瘤溶解综合征(TLS)发生在临床试验中,有些是致命的,在上市后经验中有报告,主要发生在肾细胞癌或胃肠道间质瘤患者中。通常有TLS风险的患者是那些在治疗前具有高肿瘤负荷的患者。监测这些患者的TLS并酌情管理。
7.血栓性微血管病
血栓性微血管病(TMA)包括血栓性血小板减少性紫癜和溶血性尿毒症综合征,有时会导致肾衰竭或死亡结果,发生在舒尼替尼作为单药治疗并与贝伐珠单抗联合用药的临床试验和上市后经验中。舒尼替尼未被批准与贝伐珠单抗联合使用。出现TMA的患者应停用舒尼替尼。在停用舒尼替尼后观察到TMA的作用逆转。
8.蛋白尿
已有蛋白尿和肾病综合征的报道。其中一些病例已导致肾衰竭和致命后果。监测患者蛋白尿的发展或恶化。治疗期间进行基线和定期尿液分析,并根据临床指征随访24小时尿蛋白。如果24小时尿蛋白≥3g,应中断舒尼替尼治疗并减少剂量。尽管剂量减少,但患有肾病综合征或24小时尿蛋白重复发作3g或更多的患者应停止使用舒尼替尼。尚未评估中度至重度蛋白尿患者继续接受舒尼替尼治疗的安全性。
9.皮肤毒性
⑴严重的皮肤不良反应有报道,包括多形性红斑(EM)、史蒂文斯-约翰逊综合征(SJS)和中毒性表皮坏死松解(TEN),其中一些是致命的。对于这些严重的皮肤不良反应,永久停用舒尼替尼。
⑵接受舒尼替尼治疗的患者有出现坏死性筋膜炎,包括会阴坏死性筋膜炎和继发于瘘管形成的坏死性筋膜炎。出现坏死性筋膜炎的患者应停止舒尼替尼治疗。
10.可逆性后脑白质病综合征
患者可能出现高血压、头痛、警觉性下降、精神功能改变和视力丧失,包括皮质盲。磁共振成像是确诊的必要手段。发展为可逆性后白质脑病综合征(RPLS)的患者应停用舒尼替尼。
11.甲状腺机能障碍
在临床试验和舒尼替尼的上市后经验中,均报告了甲状腺功能亢进症,有些患者随后出现甲状腺功能减退。在基线时监测甲状腺功能,在治疗期间根据临床指征定期监测甲状腺功能。在舒尼替尼治疗期间,密切监测患者甲状腺功能异常的体征和症状,包括甲状腺功能减退、甲状腺功能亢进和甲状腺炎。根据情况启动和/或调整甲状腺功能异常的治疗。
12.低血糖症
舒尼替尼可导致症状性低血糖,这可能导致意识丧失或需要住院治疗。对于正在接受舒尼替尼治疗pNET的患者,并非所有出现低血糖的患者都存在葡萄糖稳态异常。糖尿病患者的血糖水平下降可能更严重。根据临床指征并在舒尼替尼停药后定期检查基线血糖水平。对于糖尿病患者,评估是否需要调整抗糖尿病治疗以最大限度地降低低血糖风险。
13.颌骨骨坏死
⑴使用舒尼替尼治疗的患者可能发生颌骨骨坏死(ONJ),同时暴露于其他危险因素,如双膦酸盐或牙科疾病/侵入性牙科手术,可能增加ONJ的风险。
⑵在开始舒尼替尼治疗前和舒尼替尼治疗期间定期进行口腔检查。建议患者保持良好的口腔卫生习惯。如果可能的话,在预定的牙科手术或侵入性牙科手术前至少3周不使用舒尼替尼治疗。在ONJ完全解决之前,暂停治疗。颌骨骨坏死消退后恢复舒尼替尼的安全性尚未确定。
14.伤口愈合受损
有报道称,接受舒尼替尼治疗的患者伤口愈合受损。择期手术前至少停药3周。大手术后至少2周内不要给药,直到伤口完全愈合。伤口愈合并发症解决后恢复舒尼替尼的安全性尚未确定。
15.胚胎-胎儿毒性
根据动物研究结果及其作用机制,孕妇服用舒尼替尼可能会对胎儿造成伤害。告知孕妇对胎儿的潜在风险。建议有生育能力的女性在接受舒尼替尼治疗期间以及最终剂量后的4周内使用有效的避孕方法。
(七)治疗效果
1.试验设计
一项舒尼替尼在既往甲磺酸伊马替尼(伊马替尼)治疗期间出现疾病进展或对伊马替尼不耐受的GIST患者中进行的双臂、国际性、随机、双盲、安慰剂对照试验。患者随机(2:1)接受50mg舒尼替尼或安慰剂口服,每日一次,直到疾病进展或因其他原因退出研究。
2.试验结果的设定
目的是比较接受舒尼替尼联合最佳支持治疗的患者与接受安慰剂联合最佳支持治疗的患者的肿瘤进展时间(TTP)。其他目标包括无进展生存期(PFS)、客观缓解率(ORR)和总生存期(OS)。
3.试验结果
在肿瘤进展时间(TTP)中,舒尼替尼与安慰剂相比具有统计学显著优势,达到了主要终点。在方案规定的最终总生存期(OS)分析中,舒尼替尼组的中位OS为72.7周,安慰剂组为64.9周。
(八)药物相互作用
1.其他药物对舒尼替尼的影响
强CYP3A4抑制剂
与强CYP3A4抑制剂合用可能会增加舒尼替尼的血药浓度。选择无酶抑制作用或酶抑制作用最小的替代合并用药。当舒尼替尼与强CYP3A4抑制剂合用时,考虑减少其剂量。
强CYP3A4诱导剂
与强CYP3A4诱导剂合用可能会降低舒尼替尼的血药浓度。选择一种无酶诱导潜能或酶诱导潜能极小的替代合并用药。当必须与CYP3A4诱导剂合用时,考虑增加舒尼替尼的剂量。
2.延长QT间期的药物
舒尼替尼与QTc间期延长有关。对于需要使用已知可延长QT间期的合并药物进行治疗的患者,应更频繁地使用心电图监测QT间期。
(九)储存条件
将舒尼替尼储存在20℃至25℃的室温下。
【温馨提示】:部分商品说明书更换频繁,请以商品实物为准。


舒尼替尼是一种激酶抑制剂,适用于:
1.对甲磺酸伊马替尼治疗进展或不耐受的胃肠道间质瘤成人患者的治疗。
2.晚期肾细胞癌成人患者的治疗。
3.肾切除术后高危复发性肾细胞癌成人患者的辅助治疗。
4.患有不可切除的局部晚期或转移性疾病的成人患者中进行性、高分化胰腺神经内分泌肿瘤(pNET)的治疗。