格卡瑞韦/哌仑他韦(Mavyret)的中文说明书:适应症,用法用量及注意事项
格卡瑞韦/哌仑他韦是一种复方制剂,它属于直接作用的抗病毒药物,可以通过抑制丙型肝炎病毒的蛋白质复制来阻断病毒的生长和传播。这种药物已经证明在很多临床试验中具有显著的效果,可以有效地清除病毒,并且对广泛的病毒株都表现出很高的耐受性。目前格卡瑞韦/哌仑他韦已经在国内上市,本文就格卡瑞韦/哌仑他韦的适应症、用法用量、副作用、禁忌、临床疗效等进行了详细说明。
(一)适应症
格卡瑞韦/哌仑他韦适用于治疗3岁及以上患有慢性丙型肝炎病毒(HCV)基因型1、2、3、4、5或6感染但无肝硬化或代偿性肝硬化(Child-PughA)的成人和儿科患者。
格卡瑞韦/哌仑他韦适用于治疗3岁及以上的丙型肝炎病毒基因型1感染的成人和儿童患者,这些患者之前接受过含有丙型肝炎病毒NS5A抑制剂或NS3/4A蛋白酶抑制剂(PI)的治疗方案,但不能同时使用这两种药物。

格卡瑞韦/哌仑他韦
(二)推荐剂量
成人格卡瑞韦/哌仑他韦的推荐口服剂量为每日一次,每次三片且需与食物同时服用(每日总剂量:格卡瑞韦300mg和哌仑他韦120mg)。
3岁至12岁以下儿童患者的格卡瑞韦/哌仑他韦推荐剂量基于体重判断的。格卡瑞韦/哌仑他韦口服药丸建议3至12岁以下、体重小于45公斤的儿科患者使用。格卡瑞韦/哌仑他韦口服药丸是一种固定的组合药物,每包含有50mg的格卡瑞韦和20mg的哌仑他韦。
12岁及以上儿童患者,或体重至少45公斤的儿童患者,格卡瑞韦/哌仑他韦的推荐剂量为每日一次,与食物同时服用三片(每日总剂量:格卡瑞韦300mg和哌仑他韦120mg)。
(三)适用人群
成人。妊娠期、哺乳期女性,儿童以及老年患者在医生指导下用药。
(四)禁忌症
中度或重度肝功能损害(Child-PughB级或C级)患者或既往有肝功能失代偿病史的患者禁用格卡瑞韦/哌仑他韦。
格卡瑞韦/哌仑他韦禁用于阿扎那韦或利福平。
(五)副作用
在接受格卡瑞韦/哌仑他韦的受试者中,最常报告的不良反应(大于10%)是头痛和疲劳。
(六)注意事项
丙型肝炎病毒和HBV病毒共同感染患者中乙型肝炎病毒再激活的风险、晚期肝病患者的肝功能失代偿/衰竭风险、与卡马西平、含依法韦仑的方案或圣约翰草同时使用格卡瑞韦/哌仑他韦有降低疗效的风险。
(七)药物相互作用
1.格卡瑞韦/哌仑他韦对其他药物潜在作用的机制
格卡瑞韦/哌仑他韦是P-糖蛋白(P-gp)、乳腺癌耐药蛋白(BCRP)和有机阴离子转运多肽(OATP)1B1/3的抑制剂。与格卡瑞韦/哌仑他韦合用可能会增加P-gp、BCRP、OATP1B1或OATP1B3底物药物的血浆浓度。格卡瑞韦/哌仑他韦是细胞色素P450(CYP)3A、CYP1A2和尿苷葡萄糖醛酸转移酶(UGT)1a1的弱抑制剂。
2.其他药物对格卡瑞韦/哌仑他韦潜在影响的机制
格卡瑞韦/哌仑他韦是P-gp和BCRP的底物。格卡瑞韦/哌仑他韦是OATP1B1/3的底物。与抑制肝脏P-gp、BCRP或OATP1B1/3的药物合用格卡瑞韦/哌仑他韦可能会增加格卡瑞韦/哌仑他韦的血浆浓度。
与诱导P-gp/CYP3A的药物合用格卡瑞韦/哌仑他韦可能会降低格卡瑞韦和哌仑他韦的血浆浓度。
卡马西平、苯妥英、依法韦仑和圣约翰草可能会显著降低格列格卡瑞韦和哌仑他韦的血浆浓度,从而导致格卡瑞韦/哌仑他韦的治疗效果降低。不建议将这些药物与格卡瑞韦/哌仑他韦一起使用。
3.已确定的和其他潜在的药物相互作用
用直接作用的抗病毒药物清除HCV感染可能会导致肝功能改变,这可能会影响合并用药的安全有效使用。建议经常监测相关实验室参数(如服用华法林患者的国际标准化比值(INR)和糖尿病患者的血糖水平)或合并用药(如治疗指数较窄的CYPP450底物(如某些免疫抑制剂))的药物浓度,以确保安全有效使用。可能需要调整合并用药的剂量。
表4提供了格卡瑞韦/哌仑他韦对联合用药药物浓度的影响以及联合用药药物对格列卡韦和pibrentasvir的影响。所有的相互作用研究都是在成人中进行的。
表4药物相互作用研究中发现的潜在重大药物相互作用
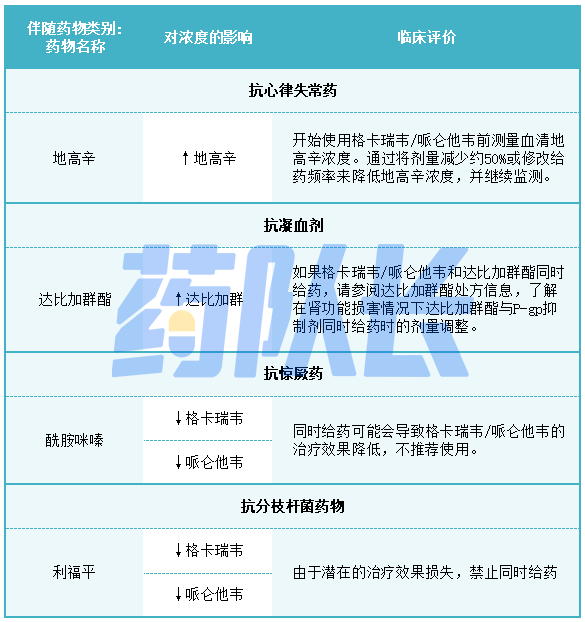
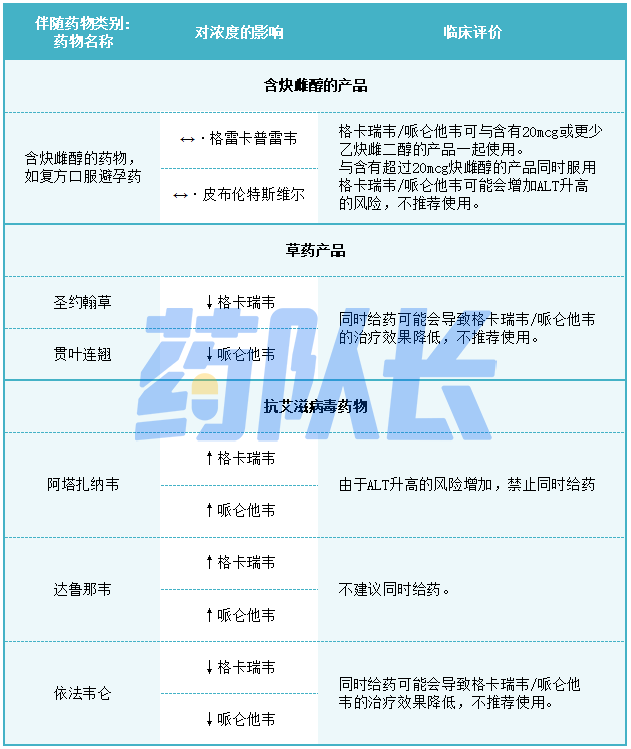
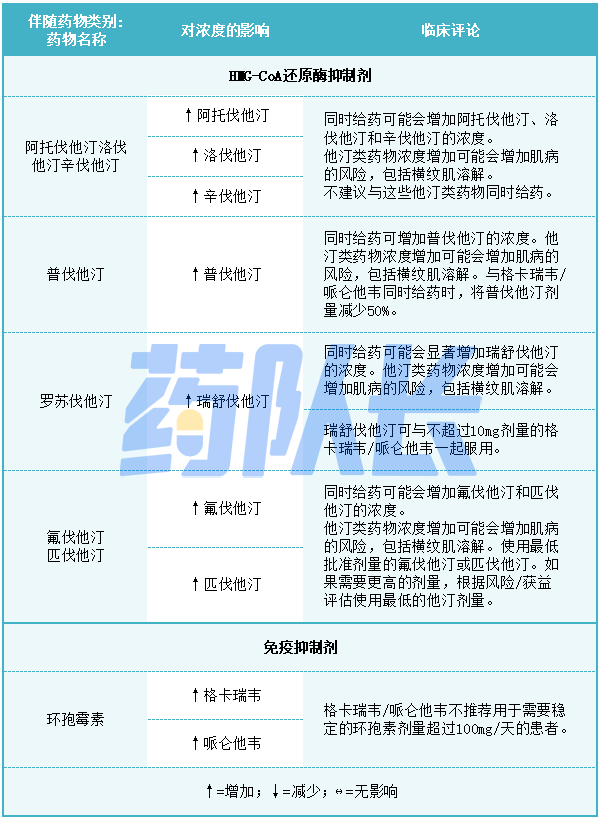
4.阿片类药物使用障碍的药物辅助治疗
与格卡瑞韦/哌仑他韦同时使用时,不需要调整丁丙诺啡/纳洛酮或美沙酮的剂量。目前没有足够的信息提供纳曲酮与格卡瑞韦/哌仑他韦合用的建议。
5.未观察到与格卡瑞韦/哌仑他韦有临床显著相互作用的药物
当格卡瑞韦/哌仑他韦与以下药物合用时,无需调整剂量:阿巴卡韦、氨氯地平、咖啡因、右美沙芬、多替格拉韦、依替格拉韦/可比司他、恩曲他滨、20μg或20μg以下的乙炔雌二醇、非洛地平、拉米夫定、拉莫三嗪、氯沙坦、咪达唑仑、炔诺酮或其他仅含孕激素的避孕药、奥美拉唑、雷替格拉韦、利匹韦林、索非布韦、他克莫司、替诺福韦阿拉芬酰胺、富马酸替诺福韦酯、甲苯磺丁脲和缬沙坦。
(八)储存条件
储存温度不超过30°C(86°F)。
【温馨提示】:部分商品说明书更换频繁,请以商品实物为准。

格卡瑞韦/哌仑他韦适用于治疗3岁及以上患有慢性丙型肝炎病毒(HCV)基因型1、2、3、4、5或6感染但无肝硬化或代偿性肝硬化(Child-PughA)的成人和儿科患者。
格卡瑞韦/哌仑他韦适用于治疗3岁及以上的丙型肝炎病毒基因型1感染的成人和儿童患者,这些患者之前接受过含有丙型肝炎病毒NS5A抑制剂或NS3/4A蛋白酶抑制剂(PI)的治疗方案,但不能同时使用这两种药物。