司美替尼(Koselugo)的用法用量
司美替尼(Koselugo)是一种可口服的、选择性的、非竞争性的ATP活性的MEK1/2抑制剂。司美替尼的用法用量需要严格遵循医生的建议。患者也需要密切关注身体状况,及时向医生反馈任何不适或异常反应。
司美替尼(Koselugo)的用法用量
1.建议用量
司美替尼的推荐剂量为25mg/m²,每日口服两次(约每12小时一次),直至疾病进展或出现不可接受的毒性。
空腹服用司美替尼。每次给药前2小时或每次给药后1小时不要进食,基于体表面积(BSA)的司美替尼推荐剂量见表1。
表1基于体表面积(BSA)的司美替尼推荐剂量

BSA小于0.55m²患者的推荐剂量尚未确定。
司美替尼胶囊整粒用水吞下。请勿咀嚼、溶解或打开胶囊。
不要给不能吞下整粒胶囊的患者服用。
除非距离下一次预定剂量超过了6小时,否则不要漏服司美替尼。
如果在服用司美替尼后出现呕吐,请不要再服用额外剂量,而是继续服用下一个计划剂量。
2.不良反应的剂量调整
表2提供了不良反应的建议剂量减少量。
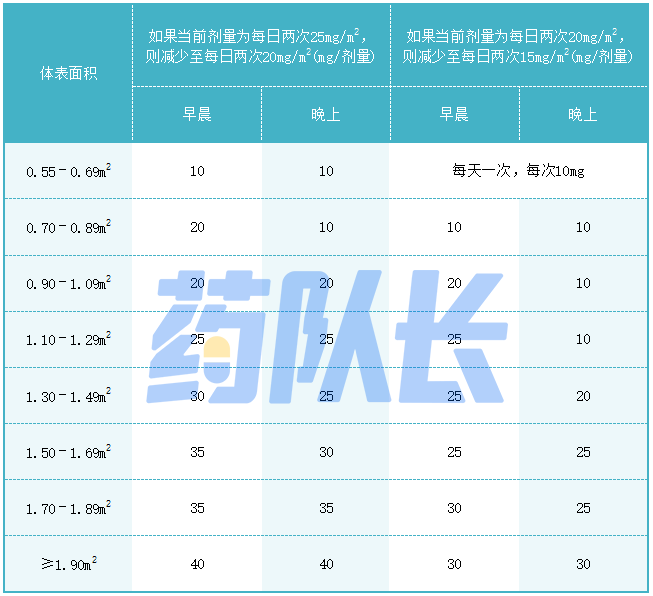
表2司美替尼不良反应的推荐减少剂量
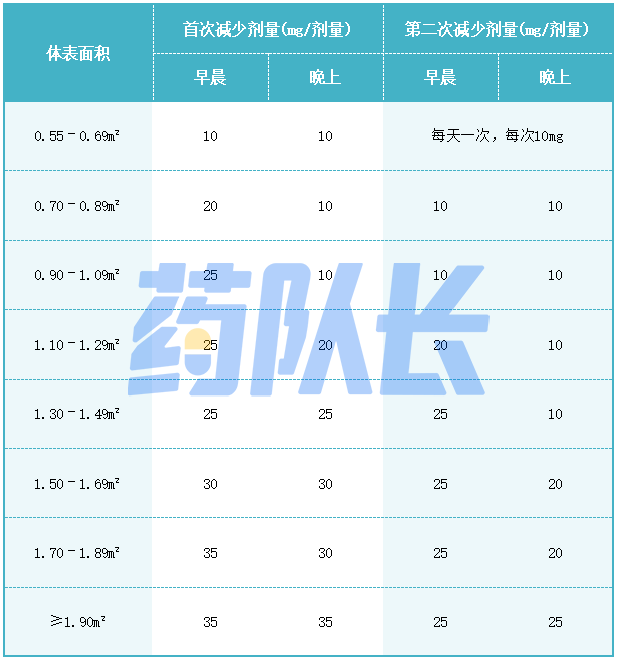
表3针对不良反应的司美替尼推荐剂量调整
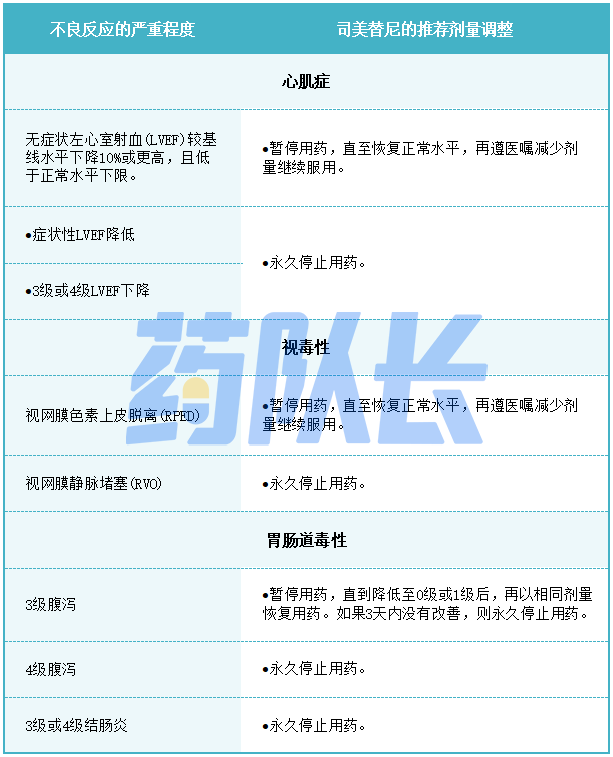
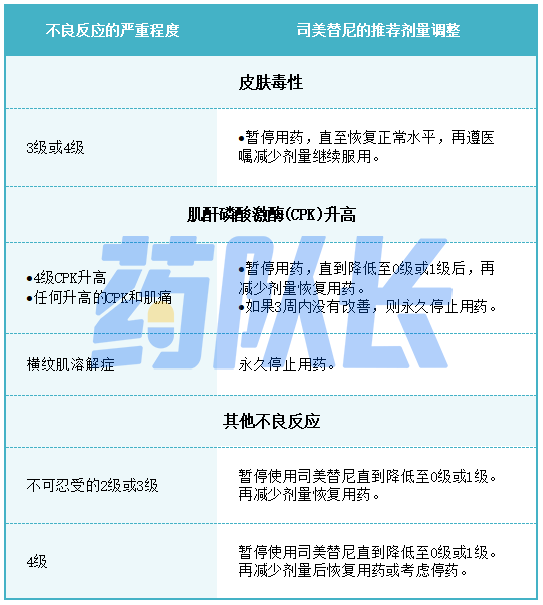
3.肝功能损害的剂量调整
中度肝功能损害患者可将司美替尼的推荐剂量降低至20mg/m²,每日口服两次(Child-PughB)。严重肝功能损害患者(Child-PughC)的司美替尼的推荐剂量尚未确定。
表4中度肝损伤的司美替尼推荐剂量
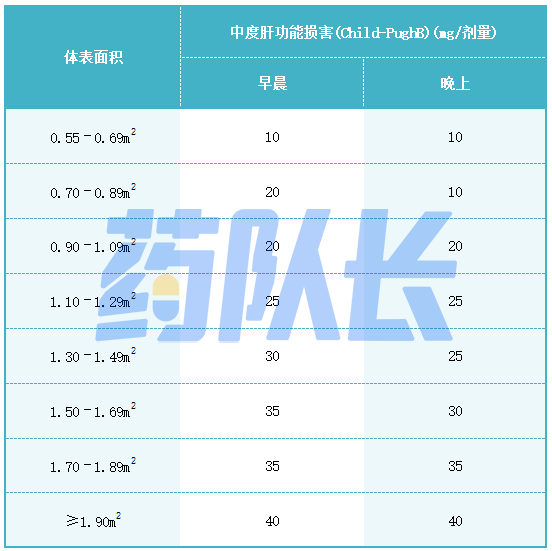
4.药物相互作用的剂量调整
强效或中度CYP3A4抑制剂或氟康唑。
避免将强效或中度CYP3A4抑制剂或氟康唑与司美替尼同时服用。如果不能避免与强效或中度CYP3A4抑制剂或氟康唑合用,则按照表5的建议减少司美替尼的剂量。停药后的强效或中度CYP3A4抑制剂或氟康唑3个清除半衰期,恢复在开始使用抑制剂或氟康唑前服用的司美替尼剂量。
表5与强效或中度CYP3A4抑制剂或氟康唑合用时的司美替尼推荐剂量

司美替尼适用于2岁及以上患有1型神经纤维瘤病(NF1)且有症状且不能手术的丛状神经纤维瘤(PN)的儿科患者的治疗。






