索托拉西布(Lumakras)的说明书
有20-30%的非小细胞肺癌患者携带KRAS基因突变,其中KRAS G12突变占KRAS突变的四成以上,且这类患者的治疗药物有限。2021年5月,美国药监局(FDA)批准索托拉西布(Lumakras)上市,适用于治疗至少接受过一次全身治疗的KRAS G12C突变、局晚期或转移性非小细胞肺癌(NSCLC)成人患者。目前索托拉西布尚未在国内上市,本文就索托拉西布的适应症、用法用量、副作用、禁忌、临床疗效等进行了详细说明。
(一)适应症
索托拉西布适用于经FDA批准的检测确认为KRAS G12C突变,且至少接受过一次全身治疗的局晚期或转移性非小细胞肺癌(NSCLC)成人患者。

索托拉西布
(二)用法用量
1.患者选择
根据患者肿瘤或血浆标本中是否存在KRAS G12C突变,选择局晚期或转移性非小细胞肺癌患者接受索托拉西布治疗。如果在血浆标本中未检测到突变,则检测肿瘤组织。
2.推荐剂量和给药方法
(1)索托拉西布的推荐剂量为960mg(320mg3片或120mg8片),每日口服一次,直至疾病进展或不可接受的毒性。
(2)每天在同一时间服用索托拉西布,可随食物同服或不同服,需整片吞下,不要咀嚼、压碎或分裂药片。如果错过一剂索托拉西布且超过6小时,请按照用药计划在第二天的规定时间服用下一剂,不要同时服用两剂索托拉西布,以弥补错过的剂量。
(3)如果在服用索托拉西布(Lumakras)后出现呕吐,不要服用额外的剂量,按照用药计划在第二天的规定时间服用下一剂。
(4)固体吞咽困难的患者用药
将片剂分散在120mL无碳酸的温水中,不要压碎,不可使用其他液体。搅拌或旋转杯子约3分钟,直到片剂分散成小块(片剂不会完全溶解),并立即或在2小时内饮用。包含索托拉西布的液体混合物可能呈现为淡黄色到亮黄色,直接吞服,不要咀嚼片剂。额外使用120mL的温水冲洗容器,然后饮用。如果不立即服用,等到服用时,请再次搅拌包含索托拉西布的液体混合物,以确保片剂分散。
3.针对不良反应的剂量调整
表1总结了索托拉西布针对不良反应的推荐减量方案,索托拉西布针对不良反应的推荐剂量调整方案见表2。如果发生不良反应,最多允许减少两次索托拉西布用量。如果患者不能耐受240mg每日一次的最低剂量,则停用索托拉西布。
表1.索托拉西布针对不良反应的推荐减量方案
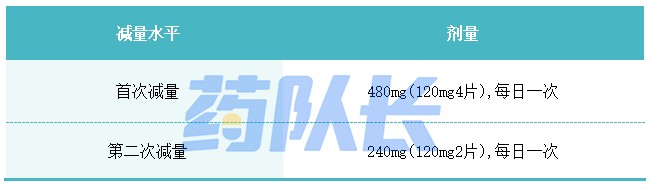
表2.索托拉西布针对不良反应的推荐剂量调整方案

a.由美国国家癌症研究所不良事件通用术语标准(NCICTCAE)5.0版定义的分级
4.索托拉西布与还原剂联合用药
应避免索托拉西布(Lumakras)与质子泵抑制剂(PPIs)和H2受体拮抗剂联合给药,如果不能避免使用抗酸剂治疗,在使用局部作用的抗酸剂前4小时或10小时后服用索托拉西布。
(三)适用人群
成人。妊娠期、哺乳期女性、严重肝功能损害患者,以及老人和儿童患者需在医生指导下用药。
(四)禁忌
尚不明确。
(五)副作用
1.最常见的不良反应(发生率≥20%)是腹泻、肌肉骨骼疼痛、恶心、疲劳、肝毒性和咳嗽。
2.最常见的实验室异常(发生率≥25%)为淋巴细胞减少、血红蛋白降低、天冬氨酸转氨酶升高、丙氨酸转氨酶升高、钙降低、碱性磷酸酶升高、尿蛋白升高和钠降低。
(六)注意事项
1.肝脏毒性
(1)使用索托拉西布可引起肝脏毒性,可能导致患者发生药物性肝损伤和肝炎。在索托拉西布开始治疗前,每3周监测一次肝功能检查[谷丙转氨酶(ALT)、谷草转氨酶(AST)和总胆红素],且在治疗的前3个月,每月监测一次或根据临床指征监测患者的肝功能检查,出现转氨酶和/或胆红素升高的患者需增加肝功能检查的频率。
(2)根据不良反应的严重程度,暂停用药、减少剂量或永久停用索托拉西布。
2.间质性肺病(ILD)/肺炎
索托拉西布可引起致命的间质性肺病/肺炎,对于疑似间质性肺病/肺炎的患者,立即停用索托拉西布,如果未发现间质性肺病/肺炎的其他潜在病因,则永久停用索托拉西布。
(七)治疗效果
CodeBreaK100试验评估了索托拉西布(Lumakras)用于KRAS p.G12C突变晚期非小细胞肺癌患者的疗效和安全性,其结果显示,接受索托拉西布治疗的患者客观缓解率(ORR)为37.1%,其中3.2%达到完全缓解(CR),33.9%达到部分缓解,并且疾病控制率高达80.6%。中位无进展生存期为6.8个月,中位总生存期为12.5个月。
安全性上,有69.8%的患者发生索托拉西布治疗相关的不良反应,其中19.8%发生3级不良事件,仅有0.8%的患者发生4级不良反应。在这项2期试验中,索托拉西布用于既往接受过治疗的KRAS p.G12C突变非小细胞肺癌患者可获得持久的临床疗效,且未出现新的不良反应。
(八)药物相互作用
1、其他药物对索托拉西布的影响
(1)抗酸剂
索托拉西布的溶解度与PH值有关,其与胃酸抑制剂联合给药会降低索托拉西布的浓度,这可能会降低索托拉西布的疗效。应避免索托拉西布与质子泵抑制剂(PPIs)、H2受体拮抗剂和局部作用的抗酸剂联合给药,如果不能避免,在局部作用的抗酸剂给药前4小时或给药10小时后服用索托拉西布。
(2)强CYP3A4诱导剂
索托拉西布是CYP3A4底物,其与强CYP3A4诱导剂联合使用会降低索托拉西布的浓度这可能会降低索托拉西布的疗效,应避免索托拉西布与强CYP3A4诱导剂联合给药。强CYP3A诱导剂包括利福平(抗结核)、利福喷丁(结核、麻风{抗金黄葡萄球菌})、苯妥英(抗癫痫、抗心律失常、三叉神经痛{精神类})、卡马西平(癫痫、三叉神经痛{镇痛药})、巴比妥(抑制中枢神经系统、抗惊厥、抗癫痫)、圣约翰草(治疗抑郁症焦虑烦躁、失眠)等。
2.索托拉西布对其他药物的影响
(1)CYP3A4底物
①索托拉西布是CYP3A4诱导剂,与CYP3A4底物联合使用可能降低其血浆浓度,这可能会降低底物的疗效。应避免索托拉西布与CYP3A4敏感性底物联合给药,因为微小的浓度变化就有可能导致底物治疗失败。
②如果不能避免联合给药,应根据处方信息增加CYP3A4敏感性底物的剂量,CYP3A4敏感性底物包括辛伐他汀、氯沙坦、咪达唑仑等。
(2)糖蛋白(P-gp)底物
①索托拉西布(Lumakras)是P-gp抑制剂,其与P-gp底物联合给药会增加其血浆浓度,这可能会增加底物相关不良反应的发生风险。应避免索托拉西布与P-gp底物联合给药,因为微小的浓度变化就有可能导致严重的毒性。
②如果不能避免联合给药,应根据处方信息减少P-gp底物的用量。
③P-gp底物包括帕唑帕尼(晚期肾细胞癌、软组织肉瘤、上皮性卵巢癌、非小细胞肺癌)、依维莫司(晚期肾细胞癌、胰腺神经内分泌瘤)、地高辛(高血压、瓣膜性心脏病、先天性心脏病、房颤、房扑、心动过速)、达比加群酯(非瓣膜性房颤患者的卒中、全身性栓塞)、利伐沙班(术后深静脉血栓和肺栓塞、非瓣膜性房颤患者的卒中、丙肝)、阿哌沙班(术后深静脉血栓)等。
(3)乳腺癌抵抗蛋白(BCRP)底物
索托拉西布是BCRP抑制剂,其与BCRP底物联合给药会增加其血浆浓度,这可能会增加底物相关不良反应的发生风险。当与索托拉西布联合使用时,应监测BCRP底物相关的不良反应,并根据处方信息减少BCRP底物的用量,BCRP底物包括甲氨蝶呤、柔红霉素、米托蒽酯等。
(九)储存条件
索托拉西布(Lumakras)为米色或黄色、椭圆形的速释薄膜包衣片剂,储存在20-25°C的室温中。
【温馨提示】:部分商品说明书更换频繁,请以商品实物为准。


适用于由FDA批准的试验确定KRAS G12C突变的且至少接受过一次全身治疗的局部晚期或转移性非小细胞肺癌(NSCLC)的成年患者