恶性血管周围上皮样细胞瘤生存时间超3年,西罗莫司白蛋白多少钱
恶性血管周围上皮样细胞瘤预后极差,晚期患者生存时间仅为12-16个月,而哺乳类雷帕霉素靶蛋白(mTOR)是其潜在的治疗靶点。2021年11月,mTOR抑制剂—西罗莫司白蛋白(Fyarro)获美国药监局(FDA)批准,可用于治疗局晚期不可切除或转移性恶性血管周围上皮样细胞瘤成人患者,该药成为FDA首个且唯一获批用于治疗成人晚期恶性血管周围上皮样细胞瘤的药物,随后获得《NCCN指南》认可,成为恶性血管周围上皮样细胞瘤的唯一首选治疗方案。本文详细描述了西罗莫司白蛋白的临床疗效、安全性和作用机制。
恶性血管周围上皮样细胞瘤预后极差,mTOR是其潜在治疗靶点
恶性血管周围上皮样细胞瘤(PEComa)是软组织肉瘤的一种罕见亚型。作为侵袭性肉瘤,该病几乎可以发生在身体的任何部位。晚期恶性血管周围上皮样细胞瘤的预后极差,此类患者的生存时间仅为12-16个月,软组织肉瘤常用的化疗对其作用不佳,患者最终多因出现远处转移导致死亡。
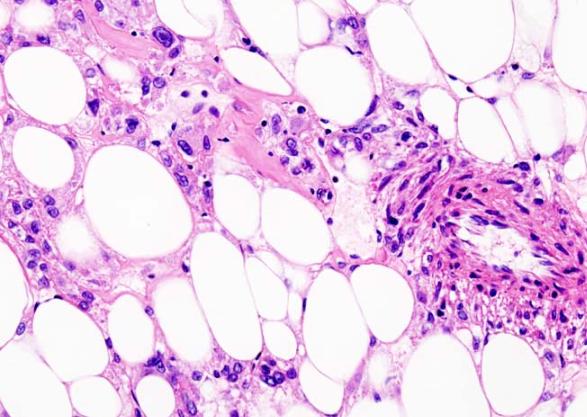
恶性血管周围上皮样细胞瘤病理图(图源于网络 侵权请告知)
在人体内TSC1和TSC2蛋白以复合体的形式抑制哺乳类雷帕霉素靶蛋白(mTOR),有研究证实在恶性血管周围上皮样细胞瘤中,存在因TSC1或TSC2基因突变导致的mTOR通路激活,导致肿瘤细胞异常增殖,因此mTOR是恶性血管周围上皮样细胞瘤潜在的治疗靶点。
mTOR抑制剂—西罗莫司白蛋白的作用机制
而由Aadi生物制药公司研发的西罗莫司白蛋白(Fyarro),正是一款mTOR抑制剂。西罗莫司白蛋白在细胞中可与FK506-结合蛋白-12(FKBP-12)受体结合,产生免疫抑制复合物,该复合物结合并抑制雷帕霉素复合物1(mTORC1)机制靶点的激活,从而减少肿瘤细胞的增殖、血管生成和葡萄糖摄取,发挥治疗作用。
西罗莫司白蛋白
罕见肉瘤首款治疗药物,西罗莫司白蛋白获批上市
2021年11月22日,美国药监局(FDA)批准西罗莫司白蛋白上市,适用于局晚期不可切除或转移性恶性血管周围上皮样细胞瘤成人患者,这代表着西罗莫司白蛋白成为FDA首个且唯一获批用于治疗成人晚期恶性血管周围上皮样细胞瘤的药物。
恶性血管周围上皮样细胞瘤获持久缓解,生存时间达40.8个月
研究人员在AMPECT试验中,探索了西罗莫司白蛋白用于局晚期不可切除或转移性恶性血管周围上皮样细胞瘤患者的临床疗效和安全性,该试验的主要终点是客观缓解率(ORR)和缓解持续时间(DOR)。
1.疗效结果
接受西罗莫司白蛋白治疗的患者客观缓解率为39%,其中有2例患者达到完全缓解(CR),尚未达到中位缓解持续时间。患者的中位无进展生存期(PFS)为10.6个月,中位总生存期(OS)为40.8个月,西罗莫司白蛋白大大延长了患者的生存时间。在出现缓解的患者中,有67%的患者缓解持续时间超过一年,58%的患者缓解持续时间超过两年。

AMPECT试验疗效结果图(图源于网络 侵权请告知)
2.安全性结果
安全性上,大多数与西罗莫司白蛋白治疗相关的不良反应为1级-2级,并且这些不良反应通过长期治疗是可以控制的,在治疗期间未发生≥4级治疗相关的不良反应。
试验证实,西罗莫司白蛋白在恶性血管周围上皮样细胞瘤患者中具有活性,可获得持久的缓解且安全性较好。
西罗莫司白蛋白在中国上市了吗?多少钱一盒?
早在西罗莫司白蛋白上市后,Aadi前首席运营官Brendan Delaney就指出西罗莫司白蛋白有望成为晚期恶性血管周围上皮样细胞瘤的标准治疗药物。2022年不负所望,西罗莫司白蛋白获得《NCCN指南》认可,成为恶性血管周围上皮样细胞瘤的唯一首选治疗方案。

Aadi前首席运营官Brendan Delaney(图源于网络 侵权请告知)
但令人遗憾的是,截止到2023年8月,西罗莫司白蛋白尚未在国内上市。目前上市地区在售的规格为100mg的西罗莫司白蛋白,参考价格为11716美元。期待它能早日踏入中国市场,为更多的罕见病家庭带来生存希望。
【温馨提示】:以上仅为参考价格,实际价格受汇率等影响可有波动。


西罗莫司白蛋白适用于治疗成人患者局部晚期不可切除或转移性恶性血管周围上皮样细胞瘤(PEComa)。