9月13日,2022欧洲肿瘤学会年会(ESMO)在法国巴黎落下帷幕,9日-13日期间,大会报告了各类肿瘤的多项新进展,其中,阿贝西利联合内分泌治疗晚期乳腺癌的数据尤其引人注目。

2022欧洲肿瘤学会年会(ESMO)宣传图
大会第一天,美国礼来(Eli Lilly)公布了MONARCH-3研究的第二次中期分析结果,该研究评估了阿贝西利联合非甾体芳香化酶抑制剂在HR+、HER2+晚期乳腺癌患者中的疗效。
据梅奥医学中心Matthew Goetz博士介绍,此次中期分析是基于对受试者长达5年的随访,结果表明,在芳香化酶抑制剂的基础上加用阿贝西利可显著改善患者的生存期,和对照组差异达12个月以上,持续证实了阿贝西利联合内分泌治疗的有效性。
HR+/HER2-乳腺癌难治,CDK4/6抑制剂+内分泌治疗效果好
乳腺癌的发病率位居全球女性恶性肿瘤首位,是造成女性癌症死亡的主要原因,因此常被称为“粉红杀手”。其中,HR+/HER2-(激素受体阳性/人表皮生长因子受体2阴性)乳腺癌是最常见的表型,占全部乳腺癌患者的60%-65%。这类乳腺癌患者的远期复发风险较高,治疗较为复杂。
内分泌治疗是HR+型晚期乳腺癌患者的首选治疗方法,传统的内分泌治疗药物类型共3种,分别为:
(1)选择性雌激素受体调节剂(SERM)(例如他莫昔芬)
(2)非甾体类芳香化酶抑制剂(NSAI)(例如来曲唑、阿那曲唑等)
(3)选择性雌激素受体下调剂(SERDs)(例如氟维司群)
然而,由于长期使用内分泌单药治疗,患者容易产生耐药性导致复发,因此急需探索联合治疗方案,以改善HR+/HER2-晚期乳腺癌患者的生存。
现存3种CDK4/6抑制剂,阿贝西利最佳
CDK4/6(细胞周期蛋白依赖性激酶4/6)抑制剂是一种新型靶向药,临床研究表明,与内分泌单一疗法相比,CDK4/6抑制剂和内分泌治疗联合可以显著延长HR+/HER2-晚期乳腺癌患者的生存期。此外,肿瘤临床诊疗指南还将内分泌治疗联合靶向药作为HR+/HER2-晚期乳腺癌患者的一线治疗推荐方案。
目前获批的CDK4/6抑制剂有3个,分别为:
(1)帕博西尼(Palbociclib)
(2)瑞博西林(Ribociclib)
(3)阿贝西利(Abemaciclib)
图左:帕博西尼,美国辉瑞,125 mg*21片;图右:瑞博西林,瑞士诺华,200 mg*63片
与其他抑制剂相比,阿贝西利对CDK4/6的选择性抑制效果更强,疗效和安全性都有所提升。
阿贝西利的作用机制
阿贝西利(Abemaciclib, Verzenio)是一种新型的口服CDK4/6抑制剂,CDK4/6是调节细胞周期的关键蛋白,阿贝西利等CDK4/6抑制剂的作用机制是抑制肿瘤细胞的有丝分裂周期,阻止其从G1期进入S期,从而起到抑制肿瘤细胞增殖的作用,为患者争取到更长的生存时间。
此外,阿贝西利是第一个被批准用于晚期乳腺癌的抑制剂,到目前为止已经在全球范围内获批多项乳腺癌适应症。
阿贝西利,美国礼来,150 mg*14片
MONARCH-1、MONARCH-2:阿贝西利治疗乳腺癌初获成果
在MONARCH-3研究之前,无论是单药治疗还是联合内分泌治疗,阿贝西利的有效性都已经得到了证实,为开展阿贝西利联合另一种内分泌治疗药物—非甾体类芳香化酶抑制研究奠定了基础,同时也为后续研究提供了安全性对照。
MONARCH-1:初步证实阿贝西利活性
MONARCH-1是第一项探究阿贝西利活性的临床试验,旨在评估阿贝西利在HR+/HER2-晚期乳腺癌患者中作为单药治疗的有效性和安全性,入组了132例既往多次治疗失败的晚期乳腺癌患者。
结果显示,阿贝西利单药治疗组患者的客观缓解率达19.7%,中位无进展生存期为6.0个月,中位总生存期为17.7个月。
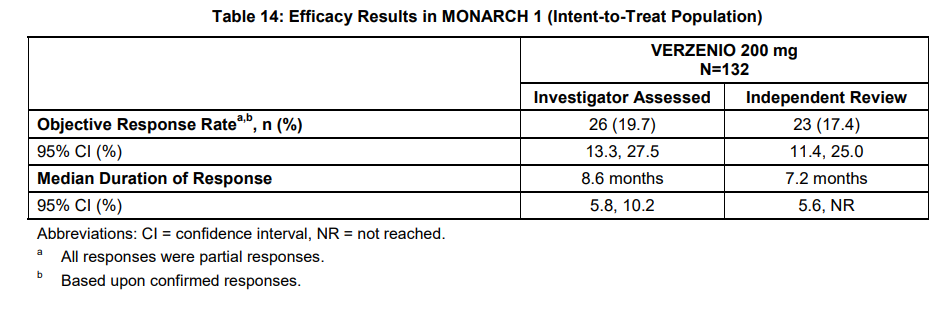
MONARCH-1研究疗效结果
MONARCH-2:初次探索阿贝西利联合内分泌治疗,二线治疗获批
MONARCH-2是第一项将阿贝西利和内分泌联合使用的3期试验,对阿贝西利或安慰剂联合氟维司群在内分泌治疗耐药后的HR阳性、HER2阴性晚期乳腺癌患者中的疗效进行了评估。
结果显示,对比安慰剂+氟维司群,阿贝西利+氟维司群组患者的中位无进展生存期更长(9.3个月 vs 16.4个月),客观缓解率显著更高(21% vs 48%)。
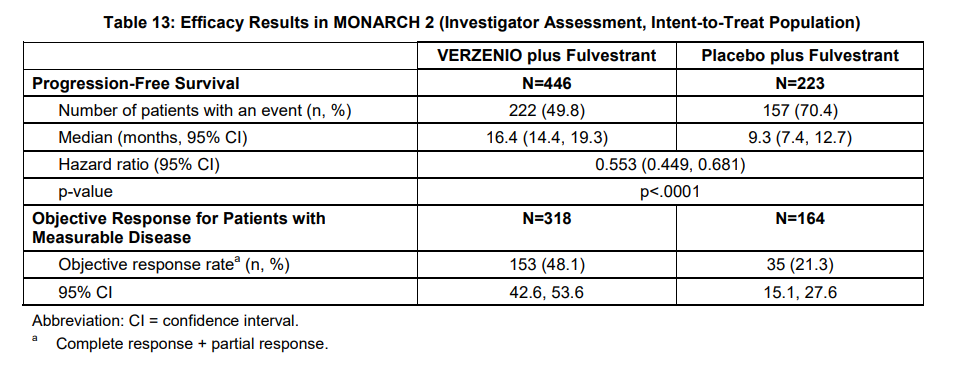
MONARCH-2研究疗效结果
基于该试验的积极结果,2017年9月,阿贝西利联合氟维司群获得美国药监局(FDA)批准用于HR+/HER2-型晚期乳腺癌患者的二线治疗。
MONARCH-3更新5年生存结果:阿贝西利+芳香酶抑制剂显著延长生存期
3期MONARCH-3试验(NCT02246621)中,评估了阿贝西利联合非甾体芳香化酶抑制剂在HR阳性、HER2阴性晚期乳腺癌绝经后女性患者中的疗效和安全性,基于该试验的积极结果,早在2018年8月份,阿贝西利就获批与芳香化酶抑制剂联合用于绝经后HR+/HER2-晚期乳腺癌患者的一线治疗,此次ESMO大会中更新了受试者的5年总体生存分析结果。
试验共纳入493例患者,按2:1的比例随机分为两组,一组(n = 328)接受150 mg阿贝西利每日两次,加1 mg阿那曲唑或2.5 mg来曲唑每日一次;另一组(n = 165)接受安慰剂加相同剂量的阿那曲唑或来曲唑。
研究的主要终点为无进展生存期(PFS),次要终点包括总生存期(OS)、疾病稳定的患者百分比和安全性等。
无进展生存期延长14.2个月
在第二次中期分析时(数据截止日期为2021年7月2日),意向治疗人群(ITT)中,接受阿贝西利+芳香化酶抑制剂治疗的患者的中位无进展生存期为29个月,而安慰剂+芳香化酶抑制剂治疗组的患者为14.8个月;
此外,阿贝西利联合治疗组保持5年无进展的患者比例为26.7%,安慰剂联合治疗组仅为9.6%。
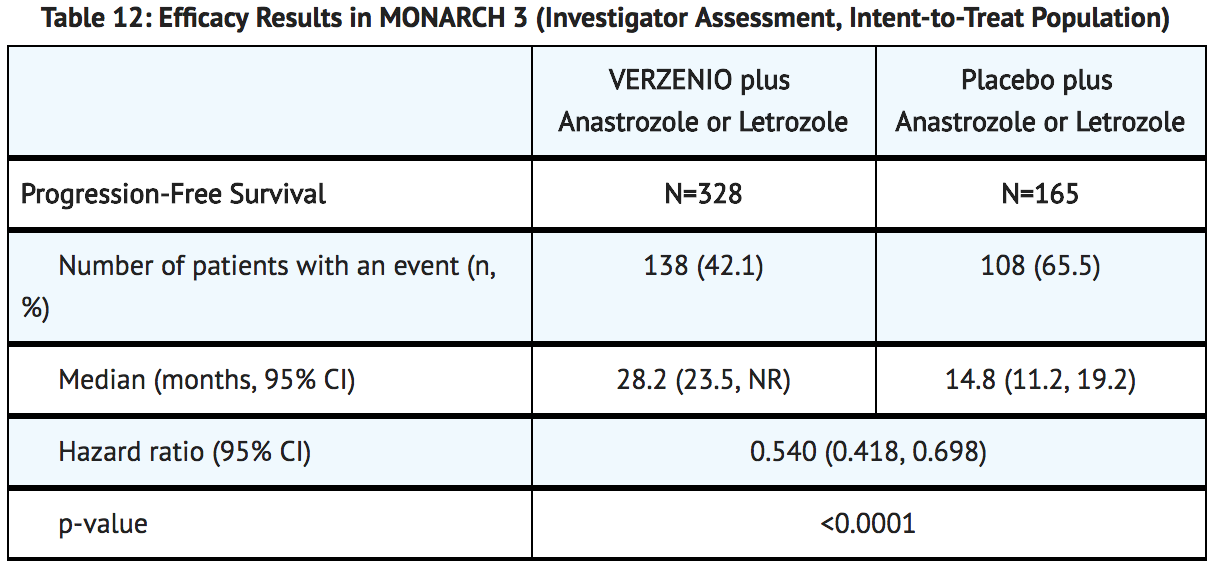
MONARCH-3研究疗效结果—中位无进展生存期
中位总生存期延长12.6个月
意向治疗人群(ITT)中接受阿贝西利+芳香化酶抑制剂治疗的患者的中位总生存期为67.1个月,接受安慰剂+芳香化酶抑制剂治疗的患者为54.5个月。
安全性和前期研究一致
在长期使用阿贝西利的患者中未观察到新的安全性信号,总体安全性特征和前期研究一致。
在接受阿贝西利联合治疗的患者中,最常见的任何级别治疗相关不良事件(TEAE)为腹泻 (83.2%)、中性粒细胞减少症(46.8%)和疲乏(44.3%);该组中最常见的≥3级TEAE为中性粒细胞减少症(27.2%)、腹泻(9.8%)和贫血(8.9%)。
阿贝西利国内已上市,医保可报销
2021年3月8日,礼来制药宣布阿贝西利(Abemaciclib)获得中国国家药监局批准上市,商品名为唯择,这是国内获批的第二款CDK4/6抑制剂,第一个在我国获批的是帕博西尼。
以下两类HR阳性、人表皮生长因子受体阴性的局部晚期或转移性乳腺癌患者可凭处方在国内医院或药房购买:
(1)与芳香化酶抑制剂联合使用作为绝经后女性患者的初始内分泌治疗
(2)与氟维司群联合用于既往内分泌治疗后出现疾病进展的患者
据查询,目前阿贝西利已被纳入2022年国家医保乙类目录,价格约为1100$每盒(150 mg)。使用医保报销后,每个月的治疗费用大概在600-1500$,由于各地医保报销比例不同,具体情况可咨询当地医保局。

阿贝西利医保状态,经国务院客户端查询
展望
阿贝西利联合芳香化酶抑制剂为晚期乳腺癌患者带来了新的治疗希望,除了这种联合方案以外,今年的欧洲肿瘤学会中也报告了很多乳腺癌领域的其他药物进展。新的药物正在不断开发,新的临床试验也在陆续开展,期待未来能为乳腺癌患者带来更多获益。
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: FDA说明书,FDA更新于2024年12月20日,https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=207103