囊性纤维化肺部功能显著改善,kaftrio多少钱一盒
囊性纤维化作为罕见的遗传性疾病,可影响产生粘液、汗液和消化液的细胞,使分泌物变得粘稠,导致肺、胰腺、肝脏等功能受损。2019年10月kaftrio(Trikafta)获批上市,适用于治疗2岁及以上的囊性纤维化患者。kaftrio由三种药物组合而成,本文详细介绍了kaftrio的临床疗效、参考价格、上市信息等。
罕见遗传性疾病—囊性纤维化
囊性纤维化(CF)是一种罕见的遗传性疾病,由特定的囊性纤维化跨膜传导调节因子(CFTR)基因出现某些突变,导致CFTR蛋白缺陷和/或缺失所引起的。而儿童必须同时遗传两个有缺陷的CFTR基因(父母各一个),才会罹患囊性纤维化。
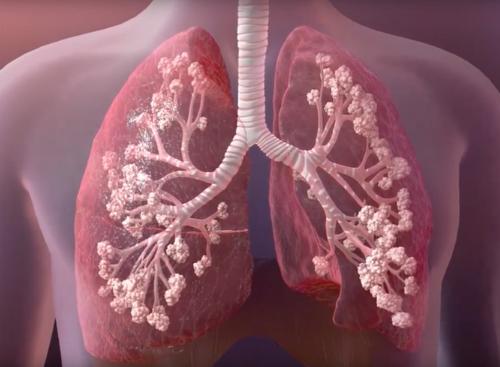
囊性纤维化示意图(图源于网络 侵权请告知)
囊性纤维化会影响产生粘液、汗液和消化液的细胞,使分泌物变得粘稠。囊性纤维化可影响肺、胰腺、肝脏等。尤其是肺部,囊性纤维化使细菌更容易粘附和繁殖,从而增加感染的风险,肺部阻塞使呼吸变得更加困难,有八成肺部疾病患者因囊性纤维化而死亡。
FDA首个囊性纤维化治疗药物—kaftrio
近年来,研究人员一直在探索治疗囊性纤维化的方法。2019年10月21日,美国药监局传来喜讯,首个治疗囊性纤维化的治疗药物—kaftrio(Trikafta)获批上市。随着适应症的进一步的扩展,kaftrio现可用于治疗CFTR基因中至少有一个F508del突变,或CFTR基因中有一个对体外数据有反应的突变且年龄在2岁及以上的囊性纤维化患者。
kaftrio
kaftrio有哪些作用?
CFTR基因约有两千种已知突变,但最常见的突变是F508del突变,约占囊性纤维化的90%。kaftrio是由elexacaftor、tezacaftor和ivacaftor组合而成,是一种突破性疗法。既可以增加细胞表面的成熟CFTR蛋白的数量,又可以改善离子通道的功能,同时还可提高运输盐和水的能力,三种药物发挥协同作用,改善囊性纤维化患者的症状。
kaftrio显著改善囊性纤维化患者的肺部功能
kaftrio的疗效已在两项临床试验中得到证实,纳入了510例至少存在一个F508del突变的12岁以上囊性纤维化患者,主要终点是用药后每秒用力呼吸量百分比(ppFEV1)变化,ppFEV1是囊性纤维化进展的标志。
1.疗效结果
在第一项试验中,与安慰剂相比,kaftrio使平均ppFEV1较基线增加了13.8%,且kaftrio改善了汗液氯化物、肺部症状加重次数(呼吸道症状和肺功能恶化)和体重指数(体重与身高之比)。在第二项试验中,与tezacaftor/ivacaftor相比,kaftrio使平均ppFEV1较基线增加了10%。
2.安全性结果
两项试验中,所有患者亚组的安全性总体相似。与安慰剂相比,接受kaftrio治疗的患者最常见的药物不良反应包括头痛、上呼吸道感染、腹痛、腹泻、皮疹、肝酶升高、鼻塞、血肌酸磷酸激酶升高、鼻漏、鼻炎、流感、鼻窦炎和血胆红素升高,更常见的严重药物不良反应是皮疹和流感。
试验证实,kaftrio显著改善了囊性纤维化患者的肺部功能,且安全性较好。基于以上数据,kaftrio获得FDA“孤儿药”认定,这意味着kaftrio为囊性纤维化患者提供了一种全新的治疗选择。
kaftrio多少钱一盒?
除了改变肺部功能,使用kaftrio的患者还发现生活质量有所改善,包括睡眠持续时间和质量提高,精力充沛和食欲增加等。kaftrio由美国VERTEX PHARMS制药公司研发,相信很多患者都很关心kaftrio的价格和上市情况。
截止到2023年9月,kaftrio尚未在中国上市,暂时没有kaftrio的仿制药,规格为75mg(ivacaftor)/50mg(tezacaftor)/100mg(elexacaftor)/片*56片,每盒约为16859美元,单片约合301美元,价格十分昂贵。我们期待kaftrio能早日踏入中国市场,纳入我国医保目录,造福更多的中国囊性纤维化患者。
【温馨提示】:以上仅为参考价格,实际价格受汇率等影响可有波动。


适用于治疗年龄在2岁及以上患者的囊性纤维化(CF),这些患者的囊性纤维化跨膜传导调节因子(CFTR)基因中至少有一个F508del突变,或CFTR基因中有一个基于体外数据有反应的突变。