2022年10月21日,美国FDA宣布已批准乌帕替尼两项新适应症的申请。在此之前,乌帕替尼主要多用于治疗类风湿性关节炎、银屑病性关节炎、特应性皮炎和溃疡性结肠炎。现已获批新适应症:强直脊柱炎和活动性非X线轴性脊椎炎。这两项新适应症的获批也是为更多的患者带来了全新的治疗选择,也开启了口服靶向治疗的新纪$。

图1.乌帕替尼说明书新增重大变化—美国FDA药品最新说明书
特应性皮炎的治疗发展史
特应性皮炎是一种慢性、具有复发性和炎症性的皮肤病,临床主要表现为反复发作的剧烈瘙痒和皮疹,患者一般会同时患有过敏性鼻炎,哮喘等其他特异性疾病,目前尚无法完全治愈。据统计。我国目前有超近3000万的特应性皮炎患者,涵盖了各大年龄层,其中,儿童、青少年和老年人为高发人群。
在乌帕替尼问世之前,我国主要采用的是外用药涂抹法、紫外线疗法、免疫抑制剂和激素等其他传统的治疗方法对特应性皮炎来进行治疗,随着生物制剂的出现,一定程度上弥补了传统的治疗手段在治疗特性性皮炎的疗效和副作用的缺口,但对于病情严重的中、重度患者,仍未很好的满足他们的治疗需求。此外,生物制剂的注射给药的方式也对患者增加了往返医院治疗的成本,给患者带来了大量的不便。[1]
在如此迫切的需求中,2019年,乌帕替尼成功的通过了FDA的审查后宣布上市。乌帕替尼的问世,为中、重度特性性皮炎的患者带来了新的治疗希望。2022年10月,乌帕替尼再次通过美国FDA审查新增了两项适应症:强直脊柱炎和活动性非X线轴性脊椎炎,为更多的患者新增了治疗的新方案。
乌帕替尼在各个国家的上市情况
2022年2月24日,中国药监局宣布乌帕替尼缓释片正式进入中国市场,用于治疗对其他系统治疗(如激素或生物制剂)应答不佳或不适应上述的治疗的成人和12岁及以上的青少年患者,临床研究数据显示,可以起到1天快速止痒、2周有效清除皮损的效果,尤其在头颈部及上肢部位的皮损展现出高效清除的优势。乌帕替尼的良好安全性,使其成为目前国内唯一获批可用于治疗青少年AD患者的JAK1抑制剂,为中重度的皮炎患者带来了新的希望。[2]
2022年7月26日,欧盟委员会(EC)批准了乌帕替尼用于治疗对常规疗法或生物制剂反应不足、反应丧失或不耐受的中重度活动性溃疡性结肠炎成人患者。
2022年7月27日,艾伯维公司向美国FDA和欧洲EMA提交了乌帕替尼一项新适应症的申请,用于治疗中重度活动性克罗恩病的成年患者。[3]
2022年10月13日,艾伯维公司宣布乌帕替尼在日本获批新适应症,用于传统治疗效果不佳的中度至重度溃疡性结肠炎成人患者的诱导缓解和维持治疗。
2022年10月21日,美国FDA宣布通过了乌帕替尼新适应症:强直脊柱炎和活动性非X线轴性脊椎炎。
乌帕替尼的新适应症:巨细胞动脉炎和Takayasu动脉炎的3期试验正在进行中,值得大家期待。
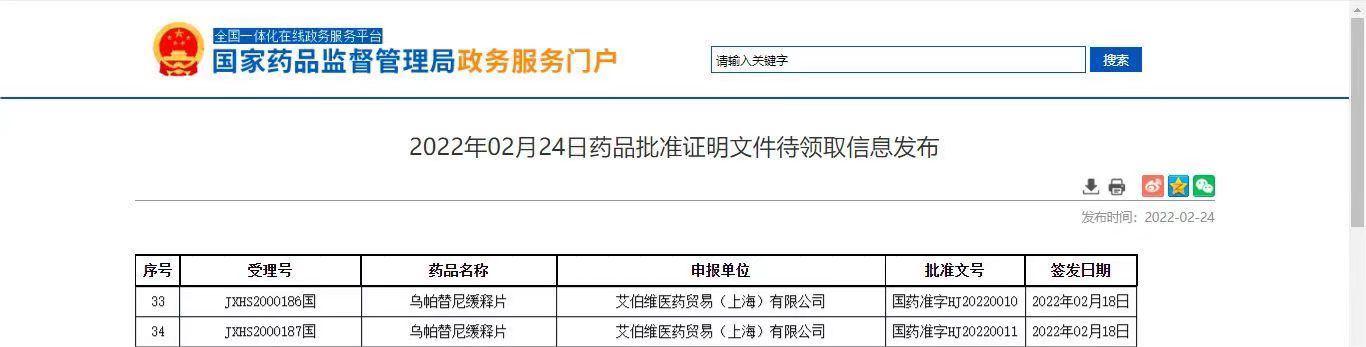
图2.2022年2月24日药品乌帕替尼批准证明文件待领取—中国药品监督管理局
乌帕替尼关于类风湿性关节炎的临床研究
试验设计
在5项3期随机、双盲、多中心研究中,对符合ACR/EULAR 2010分类标准的中度至重度活动性类风湿关节炎患者进行了15 mg 乌帕替尼每日一次的疗效和安全性评估。
试验RA-I(NCT02706873)是一项为期24周的单药治疗试验,针对947名对甲氨蝶呤(MTX)缺乏抵抗力的中度至重度活动性类风湿关节炎患者。患者接受乌帕替尼 15 mg或30 mg,每日一次或仅服用MTX单药治疗。在第26周,服用乌帕替尼的无反应患者可以通过添加MTX进行服用,而服用MTX的患者可以通过每天添加15 mg盲法或30 mg乌帕替尼进行服用。
该试验的主要终点是第12周达到ACR50反应的患者比例。主要次要终点包括疾病活动评分(DAS28-CRP)≤第12周3.2,第24周DAS28-CRP<2.6,第12周HAQ-DI基线变化,第24周范德海德修正总夏普评分(mTSS)基线变化。
试验RA-II(NCT02706951)是一项为期14周的单药试验,针对648名对甲氨蝶呤MTX反应不足的中度至重度活动性类风湿关节炎患者。患者每天接受一次15 mg或30 mg乌帕替尼单药治疗,或继续稳定剂量的MTX单药治疗。在第14周,随机接受MTX治疗的患者根据基线时预先确定的分配,以盲法提前接受15 mg 或30 mg 乌帕替尼单药治疗,每日一次。
该试验的主要终点是第14周达到ACR20应答的患者比例。主要次要终点包括DAS28-CRP≤3.2,DAS28-CRP<2.6,第14周HAQ-DI与基线相比发生变化。
试验RA-III(NCT02675426)是一项为期12周的试验,试验对象为661名中度至重度活动性类风湿关节炎患者,这些患者对传统的疾病调节性抗风湿药物(cDMARD)反应不足。患者接受15 mg或30 mg乌帕替尼,每日一次,或在背景cDMARD治疗中加入安慰剂。在第12周,随机接受安慰剂治疗的患者根据基线时预先确定的分配,以盲法提前接受15 mg或30 mg 乌帕替尼,每日一次。
该试验的主要终点是第12周达到ACR20应答的患者比例。主要次要终点包括DAS28-CRP≤3.2,DAS28-CRP<2.6,第12周HAQ-DI与基线相比发生变化。
RA-IV试验(NCT02629159)是一项为期48周的试验,对象为1629名对甲氨蝶呤MTX反应不足的中度至重度活动性类风湿关节炎患者。患者接受乌帕替尼15 mg,每日一次,活性对照,或在背景MTX中加入安慰剂。从第14周起,服用15 mg乌帕替尼的无反应患者可以盲法替换至活性对照组,服用活性对照组或安慰剂的无反应病人可以盲法替换至15 mg 乌帕替尼。在第26周,所有随机接受安慰剂治疗的患者均以盲法切换至乌帕替尼15 mg,每日一次。该试验的主要终点是与安慰剂相比,第12周达到ACR20反应的患者比例。主要次要终点包括DAS28-CRP≤3.2,DAS28-CRP<2.6,HAQ-DI在第12周从基线开始变化,mTSS在第26周从基线变化。
试验RA-V(NCT02706847)是一项为期12周的试验,针对499名中度至重度活动性类风湿关节炎患者,这些患者对生物DMARDs反应不足或不耐受。患者接受15 mg或30 mg乌帕替尼,每日一次,或在背景cDMARD治疗中加入安慰剂。在第12周,随机接受安慰剂治疗的患者根据基线时预先确定的分配,以盲法提前接受15 mg 或30 mg 乌帕替尼,每日一次。
该试验主要终点是第12周达到ACR20应答的患者比例。主要次要终点包括DAS28-CRP≤3.2,第12周HAQ-DI的基线变化。
临床反应
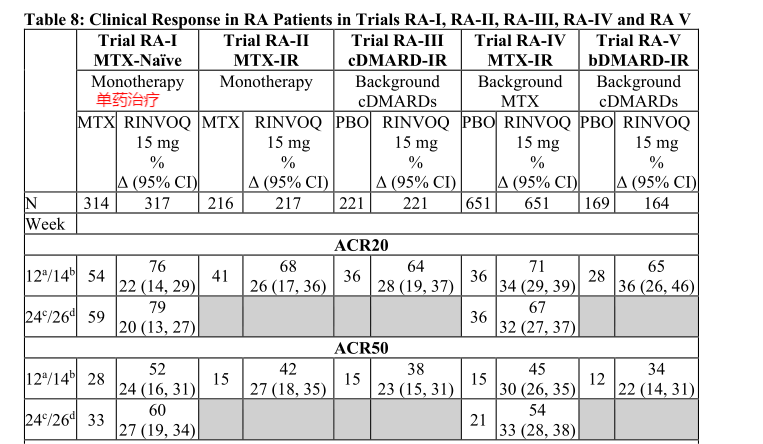
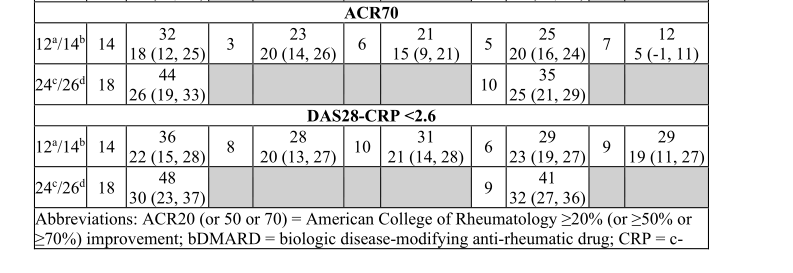
图1,1.RA-I、RA-II、RA-III、RA-IV和RAV试验中RA患者的临床反应—美国FDA药品最新说明书
注:ACR20的反应定义是:患者疼痛及肿胀关节数(28个)有20%的改善以及下列5项中至少3项的改善:①.受试者评估的疼痛(Visual Analogue Scale/Score,简称VAS)评分;②.受试者评估的疾病总体状况VAS评分;③.研究者评估的疾病总体状况VAS评分;④.健康状况问卷(Health Assessment Questionnaire,简称HAQ);⑤.急性期反应物(血沉或C反应蛋白)。ACR50、ACR70采用相同的标准分别定义为50%及70%的改善。每项指标的改善百分数=[(治疗后值-治疗前值)/治疗前值*100%]。
乌帕替尼治疗的患者在所有试验中获得ACR20、ACR50和ACR70应答以及DAS28(CRP)<2.6的百分比如上图所示,可以看出与MTX单药治疗或安慰剂相比,单独或联合cDMARD治疗15 mg 乌帕替尼的患者在主要疗效时间点分别获得了更高的ACR应答率。
在试验RA-III和RA-V中,与安慰剂相比,15 mg 乌帕替尼在1周时观察到较高的ACR20反应率通过上述可以得出,口服15mg的乌帕替尼可以较好的治疗类风湿性关节炎。
乌帕替尼关于银屑病性关节炎的临床研究
试验设计
在两项3期随机、双盲、多中心、安慰剂对照试验中,对18岁及18岁以上中度至重度活动性银屑病关节炎患者服用15 mg 乌帕替尼每日一次的疗效和安全性进行了评估。
试验PsA-I(NCT03104400)是一项为期24周的试验,研究对象为1705名中度至重度活动性银屑病关节炎患者,他们对至少一种非生物性DMARD(治疗类风湿性药物)反应或不耐受。患者接受15 mg或 30 mg的乌帕替尼,每日一次。阿达木单抗或安慰剂,单独服用或与背景非生物DMARDs联合使用作为对照组。在第24周,所有随机接受安慰剂治疗的患者均以盲法切换为15 mg 或30 mg 的乌帕替尼,每日一次。
主要研究终点是第12周达到ACR20(患者疼痛及肿胀关节数有20%的改善)反应的患者比例。
试验PsA-II(NCT03104374)是一项为期24周的试验,试验对象为642名中度至重度活动性银屑病关节炎患者,他们对至少一种生物DMARD(治疗类风湿性药物)反应或不耐受。患者接受15 mg或30 mg 乌帕替尼,每日一次。安慰剂单独服用或与背景非生物DMARDs联合使用作为对照组。在第24周,所有随机接受安慰剂治疗的患者均以盲法切换为15 mg 或30 mg 乌帕替尼,每日一次。
主要终点是第12周达到ACR20反应的患者比例。
临床反应
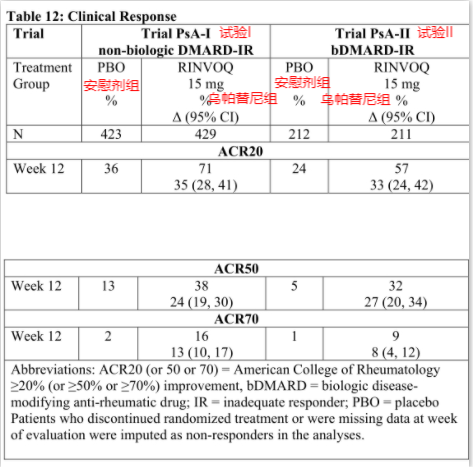
图2.乌帕替尼临床试验表格—FDA药品最新说明书
我们从图中不难看出,在上述的两项试验中,乌帕替尼组与安慰剂组相比,在第12周接受15mg的乌帕替尼治疗的患者获得了比安慰剂组高近一倍的ACR20应答。并且与安慰剂组相比,其ACR50和ACR70的应答也是远高于安慰剂。由此得出,服用15mg的乌帕替尼,对比仅服用安慰剂来说,具有很强的疗效性。
注:ACR20的反应定义是:患者疼痛及肿胀关节数(28个)有20%的改善以及下列5项中至少3项的改善:①.受试者评估的疼痛(Visual Analogue Scale/Score,简称VAS)评分;②.受试者评估的疾病总体状况VAS评分;③.研究者评估的疾病总体状况VAS评分;④.健康状况问卷(Health Assessment Questionnaire,简称HAQ);⑤.急性期反应物(血沉或C反应蛋白)。ACR50、ACR70采用相同的标准分别定义为50%及70%的改善。每项指标的改善百分数=[(治疗后值-治疗前值)/治疗前值*100%]。
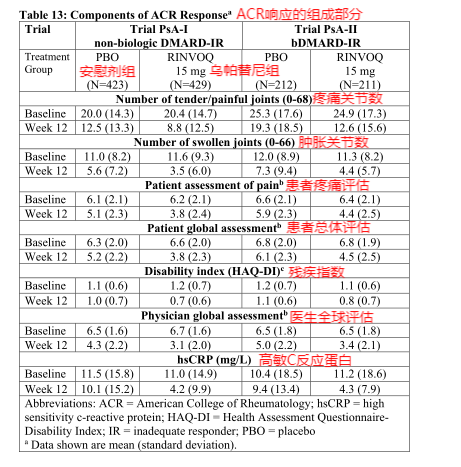
图3.乌帕替尼临床试验ACR响应组成部分—FDA药品最新说明书
从图3中我们可以得出,在服药后12周这个主要的疗效节点中,乌帕替尼组与安慰剂组相比,15mg的乌帕替尼的治疗可以较好的使ACR组成成分的改善,且改善程度远超安慰剂组。由此可得,每日服用15mg的乌帕替尼可以较好的缓解患者的银屑病性关节炎。
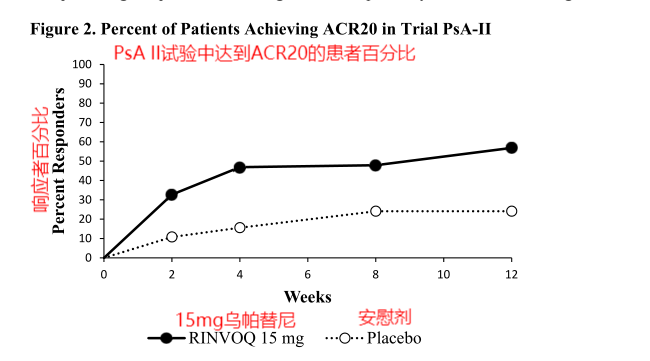
图4.PsA II试验中达到ACR20患者的百分比—FDA药品最新说明书
从图4我们可以很明显的得出,服用15mg乌帕替尼的受试组要比只服用安慰剂的对照组来说达到ACR20的响应者比率更多,即同样可以证明服用15mg的乌帕替尼可以有效的缓解治疗患者的银屑病性关节炎。
15 mg 乌帕替尼治疗可改善患者先前存在的手指炎或附着点炎患者的手指炎和附着点炎。
15 mg 乌帕替尼治疗可改善PsA患者的皮肤表现。然而,乌帕替尼尚未在斑块型银屑病中进行研究,也没有用于治疗斑块型银屑病。
特应性皮炎
试验设计
在三项3期随机、双盲、多中心试验(分别为AD-1、AD-2、AD-3;NCT03569293、NCT03607422和NCT03658318)中,对总共2584名患者(12岁及以上)进行了乌帕替尼 15 mg和30 mg每日一次的疗效评估。
在所有三项试验中,患者每天接受一次15 mg、30 mg或匹配安慰剂的乌帕替尼,持续16周。在试验AD-3中,患者还接受了乌帕替尼或安慰剂联合局部皮质类固醇(TCS)治疗16周。
上述三项试验的共同主要终点为从第 16 周的基线开始,湿疹面积和严重性指数评分 (EASI 75) 至少降低 75% 的参与者百分比和在第 16 周时,达到 0 或 1 的经过验证的研究者对特应性皮炎 (vIGA-AD) 的全球评估且从基线降低 ≥ 2 点的参与者百分比
注:vIGA-AD 是一种经过验证的评估工具,可根据以下规模评估全球特应性皮炎的严重程度:
0 - 清除:没有 AD 的炎症迹象;
1 - 几乎清晰:几乎无法察觉的红斑、硬结/丘疹和/或苔藓样变;
2 - 轻度:轻微但明确的红斑、硬结/丘疹和/或轻微的苔藓样变。没有渗出或结痂;
3 - 中度:可能存在明显可见的红斑、硬结/丘疹和/或苔藓样变、渗出或结痂;
4 - 重度:明显的红斑、硬结/丘疹和/或苔藓样变;可能存在渗出或结痂。
临床反应
单药治疗试验(AD-1和AD-2)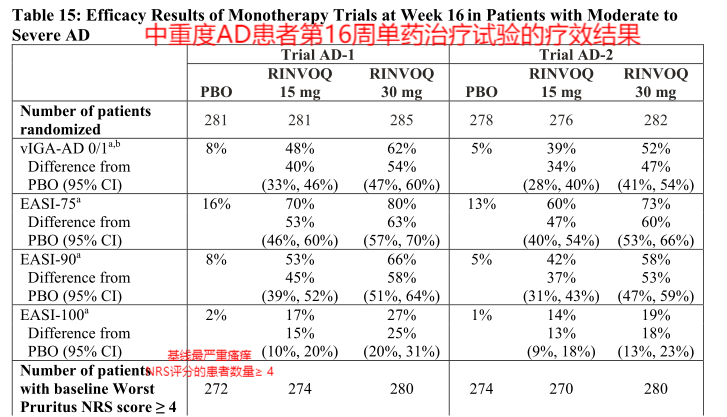
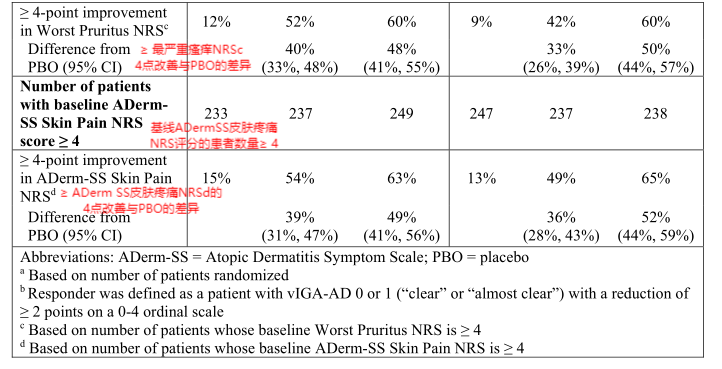
图5、6.中重度AD患者第16周单药治疗试验的疗效结果—美国FDA药品最新说明书
从图中我们可以得出主要结论:15mg乌帕替尼组的EASI 75评分为70%,30mg乌帕替尼组的EASI 75评分为80%,均远高于安慰剂组的16%。15mg乌帕替尼组的vIGA-AD0/1评分为48%,30mg乌帕替尼组的vIGA-AD0/1评分为62%,均远高于安慰剂组的8%。可以看出,在不考虑耐药和安全性的前提下,患者服用30mg的乌帕替尼的反应率>15mg的乌帕替尼>安慰剂。
合并TCS试验(AD-3)
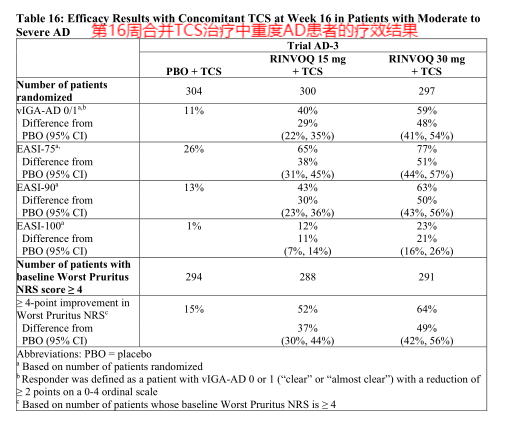
图7.第16周合并TCS治疗中重度AD患者的疗效结果—美国FDA药品最新说明书
从图中我们可以得出主要结论:15mg乌帕替尼+TCS组的EASI 75评分为65%,30mg乌帕替尼+TCS组的EASI 75评分为77%,均远高于安慰剂组的26%。15mg乌帕替尼+TCS组的vIGA-AD0/1评分为40%,30mg乌帕替尼+TCS组的vIGA-AD0/1评分为59%,均远高于安慰剂组的11%。可以看出,在不考虑耐药和安全性的前提下,患者服用30mg的乌帕替尼+TCS的反应率>15mg的乌帕替尼+TCS>安慰剂。
溃疡性结肠炎
诱导试验(研究UC-1和研究UC-2)
试验设计
在两个相同的诱导试验(UC-1;NCT02819635和UC-2;NCT03653026)中,患者被随机分为2:1,接受45 mg RINVOQ每日一次或安慰剂治疗8周。两项试验共分析了988名患者。
主要终点是第8周使用mMS确定的临床缓解。次要终点包括临床反应、内镜改善和组织学内镜粘膜改善。
注:疾病严重程度根据改良梅奥评分(mMS)进行评估,梅奥评分是一个三分量评分(0-9),由以下子评分组成(每个子评分为0-3):大便频率(SFS)、直肠出血(RBS)和集中读取的内镜评分(ES)。ES为2分的定义为明显的红斑、缺乏血管模式、易碎性和/或糜烂,评分为3分的定义是自发性出血和溃疡。
试验结果
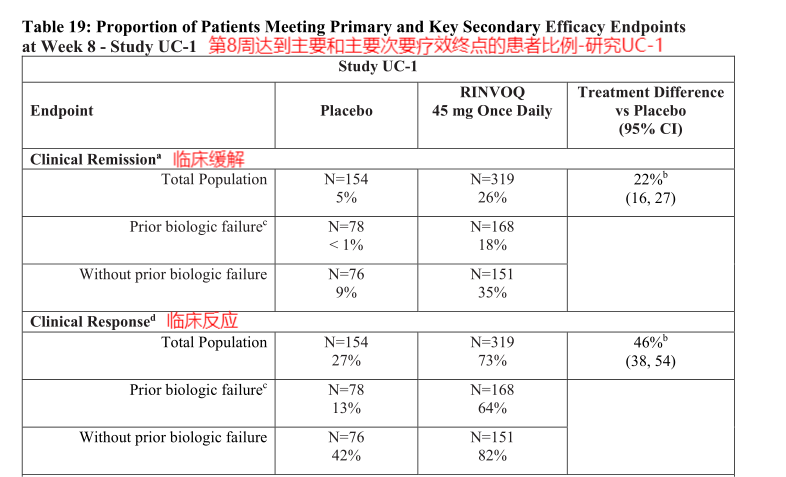
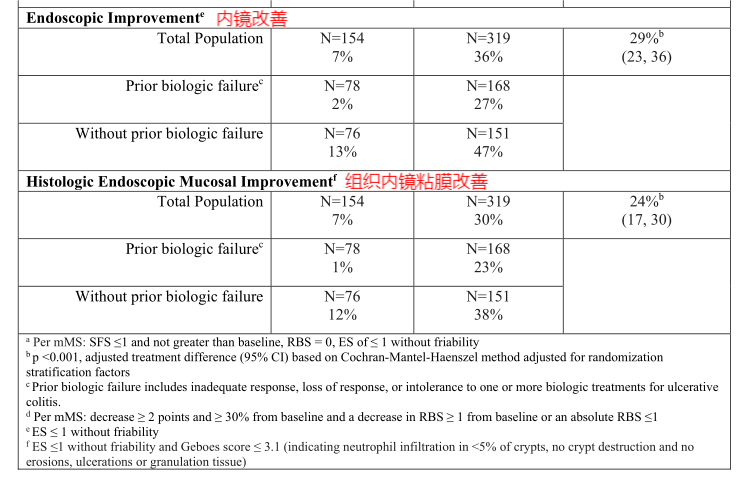
图8、9.第8周达到主要和主要次要疗效终点的患者比例-研究UC-1—美国FDA药品最新说明书
从图中我们可以简单了解,每天服用45mg乌帕替尼的受试组的临床缓解为26%,远大于安慰剂组的5%,且45mg乌帕替尼组的临床反应、内镜改善、组织内镜黏膜改善均远高于安慰剂组,由此可以得出每天服用45mg的乌帕替尼会更好的治疗溃疡性结肠炎。
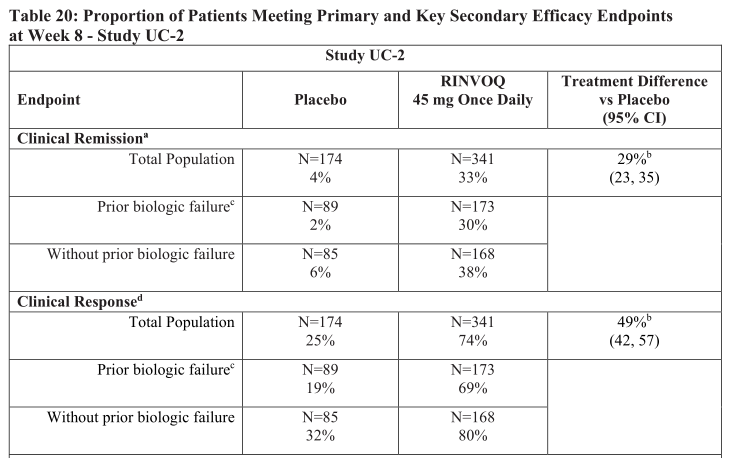
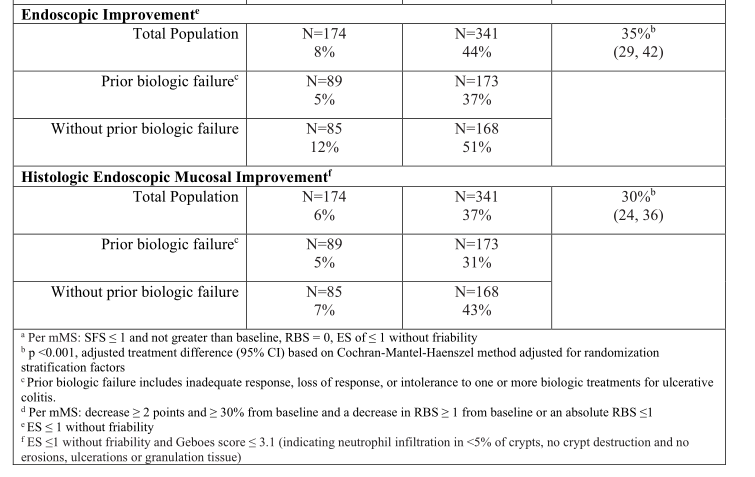
图10、11.第8周达到主要和主要次要疗效终点的患者比例-研究UC-2—美国FDA药品最新说明书
因UC-1和UC-2为除人数不同外的同样的诱导实验,结果相差不大,所以此处不再赘述。
维护研究UC-3
试验设计
在UC-3(NCT02819635)中,共有451名患者在UC-1、UC-2或UC-4中每天接受一次RINVOQ 45 mg并获得临床疗效,他们被重新随机分为每天接受15 mg、30 mg或安慰剂治疗,持续52周。
主要终点是在第52周使用mMS确定的临床缓解。次要终点包括无皮质类固醇的临床缓解、内镜改善和组织学内镜粘膜改善。
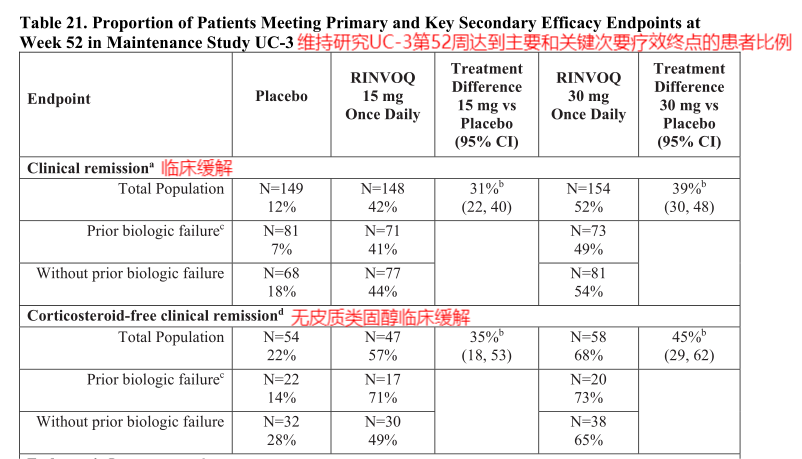
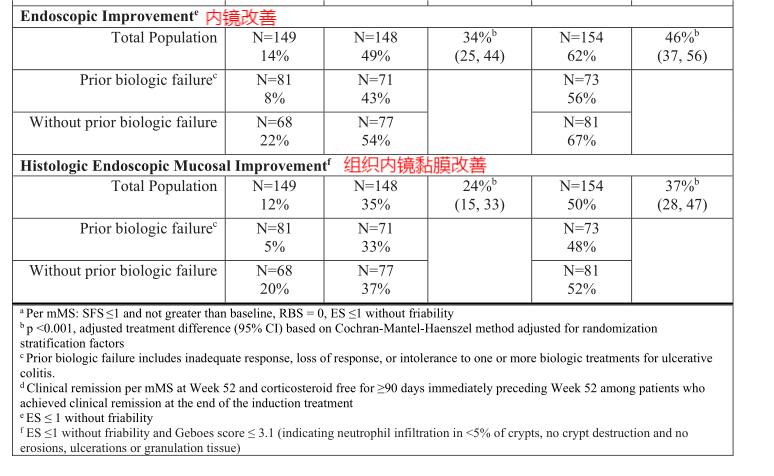
图12、13.维持研究UC-3第52周达到主要和关键次要疗效终点的患者比例—美国FDA药品最新说明书
从图中我们可以得出:每日服用30mg乌帕替尼的受试者的临床缓解为52%,每日服用15mg乌帕替尼的受试者的临床缓解为42%,均远超过安慰剂组的12%。且无皮质类固醇临床缓解、内镜改善、组织内黏膜改善均是30mg乌帕替尼>15mg乌帕替尼>安慰剂。可以很好的理解为,在不考虑副作用和耐药的前提下,每日服用30mg的乌帕替尼可以最大程度的治疗溃疡性结肠炎。
强直性脊柱炎
试验设计
根据巴斯强直性脊柱炎疾病活动指数(BASDAI),在两项随机、双盲、多中心、安慰剂对照试验中,对18岁或18岁以上的活动性强直性脊椎炎患者进行了15 mg RINVOQ每日一次的疗效和安全性评估≥4和患者对总背痛评分的评估≥4.
AS-I试验(NCT03178487)是对187名强直性脊柱炎患者进行的为期14周的试验,患者接受乌帕替尼 15 mg每日一次或安慰剂治疗。在第14周,所有随机接受安慰剂治疗的患者均改用15 mg RINVOQ,每日一次。
主要终点是在第14周达到国际脊椎关节炎协会40(ASAS40)反应评估的患者比例。
试验AS-II(NCT 04169373)是对420名强直性脊柱炎患者进行的为期14周的试验,患者接受乌帕替尼 15 mg每日一次或安慰剂治疗。在第14周,所有随机接受安慰剂治疗的患者均改用15 mg 乌帕替尼,每日一次。主要终点是在第14周达到国际脊椎关节炎协会40(ASAS40)反应评估的患者比例。
临床反应
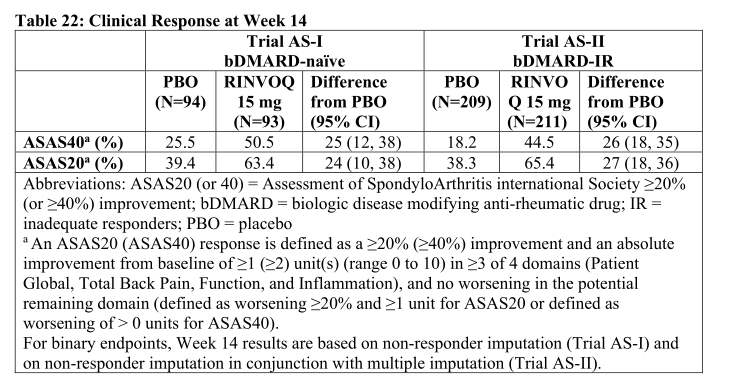
图14.第十四周的临床反应
在这两项试验中,与安慰剂相比,在第14周接受15 mg 乌帕替尼治疗的患者中,ASAS40应答的比例明显更高。在第14周,对性别、基线体重指数(BMI)和基线hsCRP的检查未发现这些亚组对乌帕替尼的反应存在差异。可以得出,每服用15mg的乌帕替尼可以较好的缓解强直性脊柱炎。
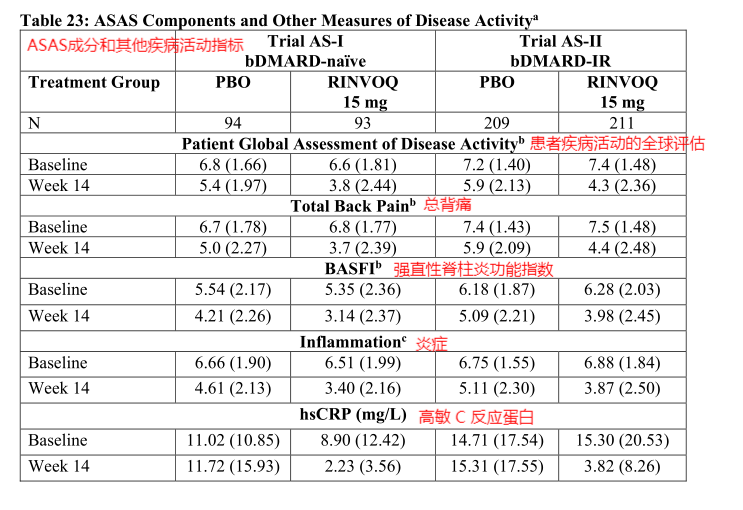
图15.ASAS成分和其他疾病活动指标—美国FDA药品最新说明书
从图中我们可以得出一个简单的结论:与安慰剂相比,15 mg 乌帕替尼治疗可改善ASAS40反应标准的各个成分。可以有效缓解强直性脊柱炎。
非X线轴性脊椎关节炎
试验设计
在一项随机、双盲、多中心、安慰剂对照试验中,对18岁或18岁以上活动性非放射轴性脊椎炎患者每天服用15 mg 乌帕替尼的疗效和安全性进行了评估。试验nr axSpA(NCT04169373)是一项为期52周的安慰剂对照试验,研究对象为314名活动性非放射轴型脊椎炎患者,患者接受乌帕替尼15 mg每日一次或安慰剂治疗。主要终点是在第14周达到国际脊椎关节炎协会40(ASAS40)反应评估的患者比例。
临床反应
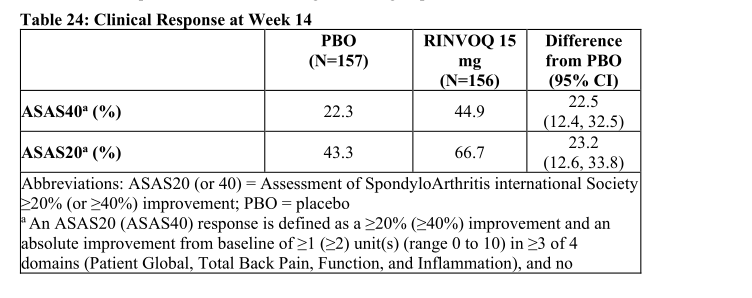
图16.第十四周的临床反应—美国FDA药品最新说明书
在试验nr-axSpA中,在第14周,接受15 mg 乌帕替尼治疗的患者中,ASAS40应答的比例为44.9%,要明显高于安慰剂组的22.3%。可以得出,每日服用15mg的乌帕替尼可以有效的缓解非X线轴性脊椎关节炎。
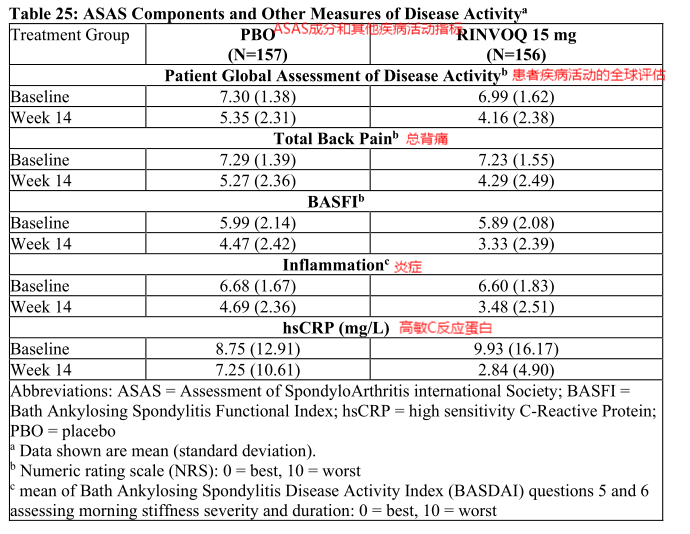
图17.ASAS成分和其他疾病活动指标—美国FDA药品最新说明书
从图中可以得出,与安慰剂相比,15 mg 乌帕替尼治疗可改善ASAS40反应标准的各个成分,可以有效的治疗非X线轴性脊椎关节炎。
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: FDA说明书,FDA更新于2024年04月16日的说明书https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=218347