温馨提示: 药品图片来自网络,仅供参考;如遇新包装上市可能存在上新滞后,请以实物为准,如有侵权,请联系删除。
本品活性成份为氟唑帕利
化学名称:4-[[3-[[2-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[1,5-α]吡嗪-7-基]羰基]-4-氟苯基]甲 基]-1(2H)-酞嗪酮
化学结构式:
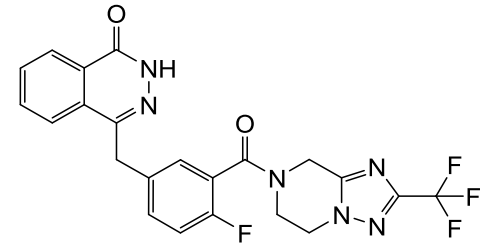
分子式:C22H16F4N6O2
分子量:472.40
本品须在有抗肿瘤治疗经验的医生指导下用药。
针对伴有胚系BRCA突变(gBRCAm)的铂敏感复发性卵巢癌:患者在服用本品治疗前,应采用国 家药监局批准的检测方法,确定患者存在有害或疑似有害的gBRCA1/2突变。
针对铂敏感复发性卵巢癌维持治疗:患者应在含铂化疗结束后的4-8周内开始本品治疗。
推荐剂量
本品推荐剂量为每次150 mg(3粒),每日服用2次(早晚各1次)。
患者在开始接受本品治疗后,应持续治疗直至疾病进展或发生不可接受的毒性反应。
给药方法
口服给药,应整粒吞服。本品在进餐后或空腹时均可服用(推荐进餐后服用)。
漏服
如果患者漏服一剂药物,应按计划时间正常服用下一剂量。
剂量调整
针对不良事件
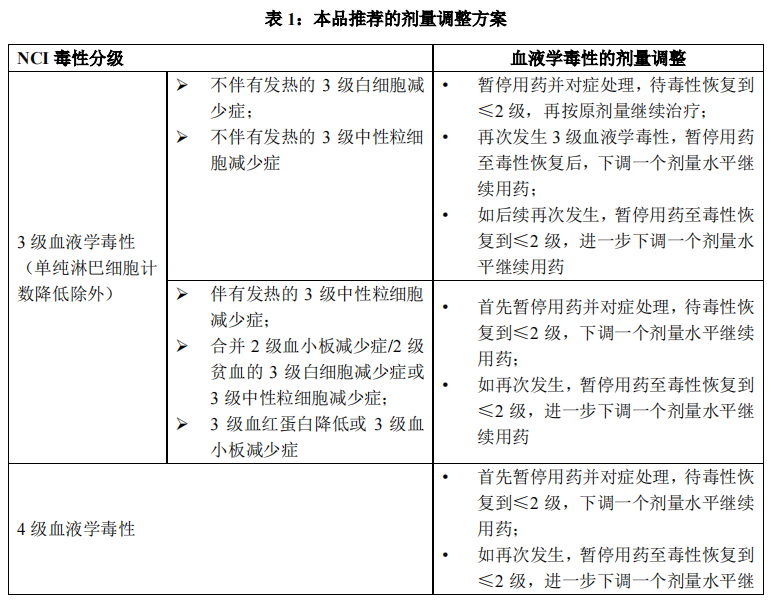
为处理不良事件,可参见表1进行减量或暂停用药。
如果需要减量,推荐首先从每次150 mg(3粒)减至每次100 mg(2粒),每日服用2次。
如果需要进一步减量,则推荐从每次100 mg(2粒)减至每次50 mg(1粒),每日服用2次
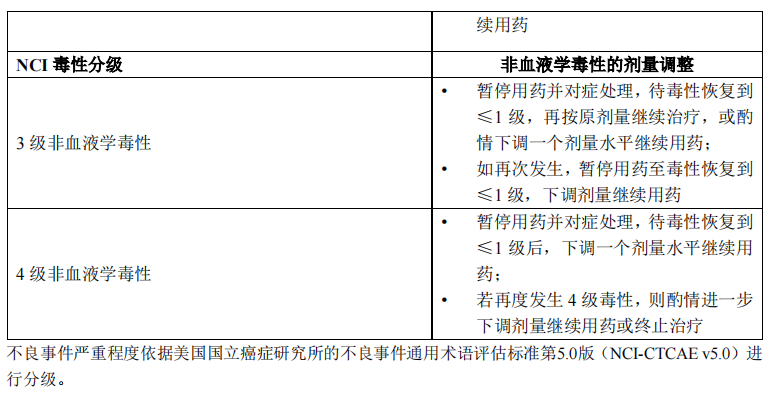
合并使用细胞色素P4503A4(CYP3A4)抑制剂
本品治疗期间避免合并使用CYP3A4强抑制剂。如必须使用,可以停用氟唑帕利;在停止合并使用CYP3A4强抑制剂且至该药物清除5-7个半衰期后,可恢复氟唑帕利至原给药剂量和频率。如与CYP3A4中等抑制剂合用时,建议下调氟唑帕利剂量至50mg。
特殊人群
肝功能损害
轻度肝功能损害对氟唑帕利清除率未观测到显著影响,轻度肝功能损害(根据美国国家癌症研究所(NationalCancerInstitute,NCI)-器官功能障碍工作组(OrganDysfunctionWorkingGroup,ODWG)标准)患者服用本品无需进行额外剂量调整。
中重度肝功能损害患者使用本品的安全性和有效性尚不明确。在获得更多信息前,不建议中重度肝功能损害患者使用本品。
肾功能损害
轻度肾功能损害对氟唑帕利清除率未观测到显著影响,轻度肾功能损害(肾损伤程度由肌酐清除率CLCR决定,可通过Cockcroft-Gault方程进行估算)患者服用本品无需进行额外剂量调整。
中重度肾功能损害患者使用本品的安全性和有效性尚不明确。在获得更多信息前,不建议中重度肾功能损害患者使用本品。
儿童或青少年
尚未确立本品在18岁以下患者中的安全性和疗效。不推荐18岁以下患者使用。
老年人群
本品目前在>65岁的老年患者中应用数据有限,建议在医生的指导下使用。
在上述接受氟唑帕利单药治疗的294例患者中,所有级别的不良反应发生率为96.3%,下文以及表2所列的不良反应发生率是所有已报告的基于研究者评估的药物不良反应。
最常见的不良反应(发生率≥10%)
贫血(62.2%)、恶心(59.5%)、白细胞减少症(57.5%)、乏力(45.2%)、血小板减少症(45.6%)、中性粒细胞减少症(40.8%)、呕吐(26.9%)、食欲减退(23.5%)、淋巴细胞减少症(21.8%)、血肌酐升高(21.1%)、ALT升高(10.5%)。
最常见的≥3级不良反应(发生率≥2%)
贫血(27.9%)、血小板减少症(14.3%)、中性粒细胞减少症(11.2%)、白细胞减少症(11.2%)和淋巴细胞减少症(6.1%)。
血液学毒性
在接受本品治疗的患者中报告了血液学毒性,包括贫血、白细胞计数降低、中性粒细胞计数降低、血小板计数降低和淋巴细胞计数降低等临床诊断和/或实验室检查结果。既往抗肿瘤治疗引起的血液学毒性未恢复之前(血红蛋白、血小板和中性粒细胞水平应恢复至≤1级),患者不应开始接受本品治疗。在治疗最初的3个月内,推荐在基线进行全血细胞检测,随后每2周监测一次,之后定期监测治疗期间出现的具有临床意义的参数变化(见【不良反应】)。
如果患者出现重度或输血依赖性的血液学毒性,应中断治疗,并且应进行相关的血液学检测。
如果本品给药中断4周后血液指标仍存在临床异常,则推荐骨髓分析和/或血细胞遗传学分析。
针对心脑血管高危患者,需要加强贫血相关监测,必要时进行剂量调整。
骨髓增生异常综合征/急性髓系白血病
骨髓增生异常综合征/急性髓系白血病(MDS/AML)在PARP抑制剂治疗肿瘤的临床研究中有报道,部分事件结局为死亡。MDS/AML发生的时间为接受PARP抑制剂数月至数年不等,患者存在既往接受含铂化疗,和/或其他DNA损伤药物治疗包括放疗。部分患者有骨髓发育不良的病史。
在氟唑帕利临床研究中尚未报告此类事件发生。在实际使用过程中,应密切监测MDS/AML的症状、体征和实验室检查结果。一旦确诊应永久停药,并进行适当的治疗。
胚胎-胎儿毒性
根据本品的作用机制(聚ADP核糖聚合酶抑制)及动物试验,当妊娠女性服用本品时,可能对胎儿造成伤害。
在妊娠期间不应服用本品。如果患者在服用药物期间怀孕,应告知患者本品对胎儿潜在的危害。
建议育龄期女性在治疗期间以及最后一次服药后6个月内必须使用有效的避孕措施。
对驾驶和操作机器能力的影响
本品可能出现乏力等不良反应(参见【不良反应】),出现这些症状的患者应谨慎驾驶或操作机器。
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm。
- 药品知识
- 药品信息
-
【青光眼或高眼压症】DE-117B滴眼液
[适应症]原发性开角型青光眼或高眼压症[试验分期]Ⅲ期
-
【肝功能不全】LH-1801片
[适应症]肝功能不全[试验分期]Ⅰ期
-
【系统性红斑狼疮】C-CAR168细胞回输注射液
[适应症]系统性红斑狼疮[试验分期]Ⅱ期
-
【复发脑胶质瘤】GNC-039四特异性抗体注射液
[适应症]复发脑胶质瘤(病理确诊为四级星型细胞瘤和四级胶质母细胞瘤)[试验分期]Ⅰ期