
 请您输入药品名
请您输入药品名

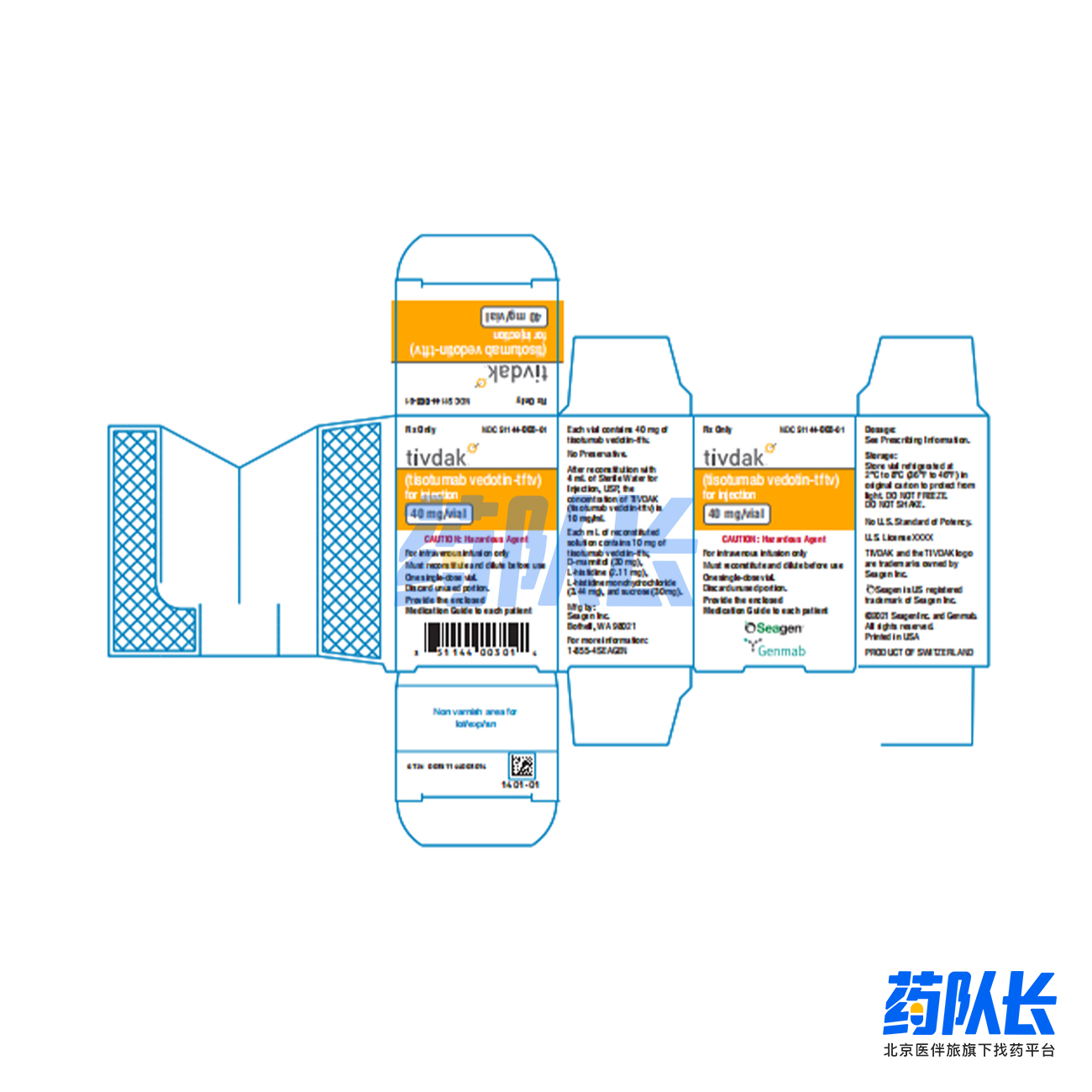
替索单抗
![$drugs['manufacturersinfo']['name'].jpg](https://m.1blv.cn/upload/default/20220420/cd3ddaba94402b3ec87a16bff64b062.jpg) 美国seagen
美国seagen ADC药物,治疗复发或转移性宫颈癌中位缓解持续8.3个月
-
别名:Tivdak、Tisotumab、vedotin-tftv

-
剂型:冻干粉
-
规格:40mg
-
有效期:36个月
-
上市时间:2021年9月
1、眼部不良反应
(1)临床试验中,使用本品后有出现眼部不良反应的报道,因此将患者转介给眼科护理提供者进行眼科检查,包括在基线、每次剂量前和临床需要时的视力和裂隙灯检查,坚持用药前和必要的眼部护理,以减少眼部不良反应的风险;
对于任何新的或恶化的眼部体征和症状,及时将患者转介给眼科护理提供者
(2)根据不良反应的严重程度,暂停、减少剂量或永久停用本品
2、周围神经病
监测患者的神经病变体征和症状,如感觉异常、刺痛或烧灼感、神经性疼痛、肌肉无力或感觉异常;
对于出现新的或恶化的外周神经病变的患者,根据外周神经病变的严重程度,暂停给药,然后减少剂量或永久停用Tivdak
3、出血
(1)监测患者有无出血的体征和症状,对于出现肺部或中枢神经系统出血的患者,应永久停用Tivdak
(2)对于任何其他部位的≥2级出血,应暂停治疗,直到出血消退,血红蛋白稳定,没有可能增加继续治疗风险的出血因素,也没有可能增加出血复发风险的解剖或病理条件
(3)解决后,恢复治疗或永久停用Tivdak
4、肺炎
监测患者是否出现肺炎的肺部症状;
在放射学检查中,症状可能包括缺氧、咳嗽、呼吸困难或间质浸润,应通过适当的调查排除此类症状的传染性、肿瘤性和其他原因
对于出现持续性或复发性2级肺炎的患者,停止使用Tivdak,并考虑减少剂量;
对所有3级或4级肺炎患者永久停用Tivdak
5、胚胎-胎儿毒性
告知患者对胎儿的潜在风险,建议具有生殖潜力的女性在接受Tivdak治疗期间以及最后一次给药后的2个月内使用有效的避孕措施;
建议具有生殖潜力的女性伴侣的男性患者在使用 Tivdak治疗期间以及最后一次给药后的4个月内使用有效的避孕方法
(以上内容参考自美国FDATivdak说明书2021.09版)
 4001551018
4001551018

 德国默克
德国默克 
 瑞士罗氏
瑞士罗氏 
 孟加拉珠峰
孟加拉珠峰 









