温馨提示: 药品图片来自网络,仅供参考;如遇新包装上市可能存在上新滞后,请以实物为准,如有侵权,请联系删除。
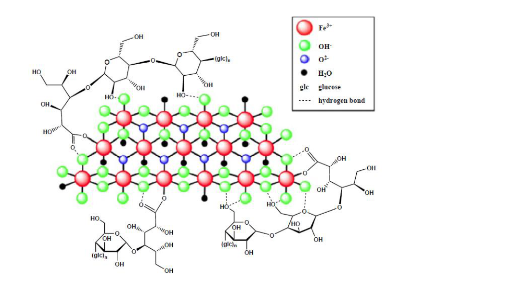
本品主要成分为:Injectafer,化学结构式为:
推荐剂量
1、对于体重≥50kg的患者,推荐剂量为750mg,分2次静脉注射,间隔至少7天,每个疗程的总累积铁剂量为1500mg;对于体重≥50kg的患者,可在一个单剂量疗程中静脉注射15mg/kg体重的替代剂量,最高可达1000mg
2、对于体重<50kg的患者,推荐剂量为15mg/kg体重,分2次静脉注射,间隔至少7天
3、每毫升注射剂含有50mg元素铁
准备和管理
1、可以直接静脉注射,也可以是未稀释的缓慢静脉推注,也可以是输注;当通过输注给药时,在不超过250ml无菌0.9%氯化钠注射液(USP)中稀释1000mg,使得输注浓度不低于每ml2mg铁,并在至少15 分钟内给药
2、当加入到含有 0.9%氯化钠注射液(USP,浓度范围为每ml/2mg-4mg铁)的输液袋中时,注射液溶液在室温下储存72小时时物理和化学稳定;为保持稳定性,请勿稀释至低于2mg铁/ml的浓度
3、给药前,目视检查注射用药物是否存在颗粒物质和变色,该产品不含防腐剂,每瓶Injectafer仅供单剂量使用
4、750mg注射剂缓慢静脉推注时,以每分钟约 100mg(2ml)的速度给药;对于1000mg的注射剂,在15分钟内缓慢静脉推注;避免注射液外渗,因为外渗部位的褐色变色可能会持续很久,因此需监控外渗情况,如果发生外渗,在该部位停止注射
5、丢弃未使用的部分
最常见的不良反应(>2%)是恶心、高血压、脸红、注射部位反应、红斑、低磷血症和头晕
儿科患者最常见的不良反应(≥4%)是低磷酸盐血症、注射部位反应、皮疹、头痛和呕吐
1、过敏反应
接受Injectafer治疗的患者曾出现过严重的过敏反应,其中一些反应会危及生命和死亡,患者可能出现休克、临床上明显的低血压、意识丧失和/或虚脱
因此在注射过程中和注射后至少30分钟内监测患者的过敏症状和体征直至输注完成后临床症状稳定,仅在人员和疗法可立即用于治疗严重过敏反应时,才使用本品
2、症状性低磷酸血症
接受本品治疗的患者可能会出现症状性低磷血症,在开始使用Iniectafer进行治疗之前,纠正原有的低磷血症,监测慢性低血磷风险患者的血磷水平;对于有低血清磷酸盐风险的患者和在三个月内接受第二个疗程的任何患者,在重复疗程前检查血清磷酸盐水平,根据医学指征治疗低磷酸盐血症
3、高血压
使用本品可能会出现高血压,部分患者可能会出现面部潮红、头晕或恶心,这些表现通常在给药后会立即出现,并在30分钟内消失,因此每次注射后监测患者的高血压体征和症状
4、实验室测试变更
在注射后 24小时内,实验室化验可能会高估血清铁和转铁蛋白结合铁,因为也测量注射后的铁
(以上内容参考自美国FDA Injectafer说明书2023.5版)
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表药队长立场,亦不代表药队长支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm。
- 药品知识
- 药品信息
- 喜讯!Injectafer成为FDA首款缺铁性心衰静脉铁剂 继2013年FDA首次批准Injectafer用于治疗口服铁剂疗效不满...[ 详情 ]推荐指数:1074 2023-06-15
-
【青光眼或高眼压症】DE-117B滴眼液
[适应症]原发性开角型青光眼或高眼压症[试验分期]Ⅲ期
-
【肝功能不全】LH-1801片
[适应症]肝功能不全[试验分期]Ⅰ期
-
【系统性红斑狼疮】C-CAR168细胞回输注射液
[适应症]系统性红斑狼疮[试验分期]Ⅱ期
-
【复发脑胶质瘤】GNC-039四特异性抗体注射液
[适应症]复发脑胶质瘤(病理确诊为四级星型细胞瘤和四级胶质母细胞瘤)[试验分期]Ⅰ期






